
Fig.1
ALMACÉN
Determinación de la masa molar del oxígeno
Aproximación al Número de Avogadro
Determinación del número de moléculas de agua de cristalización de una sal
Cinética de la reacción del ión tiosulfato en medio ácido
Punto de congelación de una mezcla de naftaleno y paradiclorobenceno
Calor de neutralización de un ácido fuerte con una base fuerte
Cinética de la reacción entre los iones peroxodisulfato y los iones yoduro
Estequiometría de la reacción entre el ácido clorhídrico y el mármol
Estequiometría de la reacción entre el yoduro potásico y el nitrato de plomo(II)
Cinética química de la reacción entre los iones yodato e hidrógenosulfito
Iniciación a las masas relativas y al mol
Redox con tartrato, agua oxigenada y sulfato de cobre(II)
Reacción entre el cloruro de estaño(II) y el cloruro de mercurio(II)
Reacción del sodio con el agua
Electrólisis del cloruro de estaño(II)
Cristales de sulfato de cobre(II)
Introducción a los potenciales redox
Reacción entre el permanganato potásico y glicerina
Reacciones de precipitación de sales de plata(I)
Reacciones de precipitación de sales de plata(II)
Reacciones de precipitación de sales de plata(III)
Reacciones de precipitación de sales de plata(IV)
Reacciones de precipitación de sales de Hg(II) y Cu(II), I
Reacciones de precipitación de sales de Hg(II) y Cu(II), II
Reacciones de precipitación del Fe(III), I
Reacciones de precipitación del Fe(III), II
Reacciones de precipitación del Fe(II)
Reacciones de precipitación del Ni(II)
Reacciones de precipitación de hidróxidos I
Reacciones de precipitación de hidróxidos II
Reacciones de precipitación del Co(II) Primera parte
Reacciones de precipitación del Co(II) Continuación
Reacciones de precipitación del Hg(I)
Reacciones de precipitación del Hg(II)
Reacciones de precipitación del Pb(II).Primera parte
Reacciones de precipitación del Pb(II). Final
Reacciones de precipitación del Ba(II).Primera parte
Reacciones de precipitación del Ba(II).Continuación
GRUPO HEUREMA. EDUCACIÓN SECUNDARIA
ENSEÑANZA DE LA FÍSICA Y LA QUÍMICA

Fig.1
ALMACÉN

Fig.3

Fig.2

Fig.10
Reacciones de
precipitación 21
Precipitación del Cd(II).
21.1. Precipitación
del hidróxido de cadmio
Primeramente sobre una disolución de cloruro de cadmio, echamos unas gotas de disolución de hidróxido sódico 6N, formándose un precipitado blanco de hidróxido de cadmio (Oscila según los textos entre los valores Kps=1,6.10-14-7,2.10-15), que toma formas muy curiosas como se puede apreciar (fig.1-4). La sucesión de fotos está hecha con un intervalo de 0,3 segundos.
21.3. Precipitación del sulfuro de cadmio
Si la disolución saturada de cloruro de cadmio se trata ahora con otra de sulfuro sódico, precipita el sulfuro de cadmio (Según textos Kps=1,1.10-25-1.10-27), primero forma una capa superficial blanquecina, (fig.10) que se irá poco a poco depositando en el fondo (Fig.11-13). La sucesión de fotos 10-13. está hecha con un intervalo de 0,3 segundos.
La reacción química que se produce es :
Na2S+CdCl2 → CdS(precipitado blanco grisáceo) +2NaCl

Fig.5

Fig.9 (ampliación)
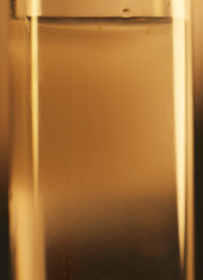
Fig.12

Fig.13

Fig.8(ampliación)

Fig.7

Fig.6 (detalle)
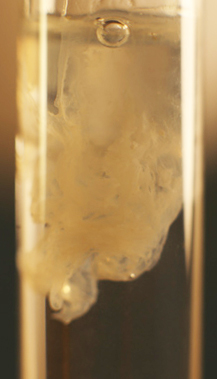
Fig.4
La reacción química que se produce es :
K2CrO4+CdCl2 → CdCrO4 (precipitado amarillo) +2KCl
21.2. Precipitación del cromato de cadmio
Otra precipitación es en forma de cromato de cadmio (Kps=1,2.10-9), primero forma una capa superficial, que se irá poco a poco depositando en el fondo (Fig.5-9). La sucesión de fotos 5-9. está hecha con un intervalo de 0,3 segundos.

Fig.11
La reacción química que se produce es :
H2SO4+CdCl2 → CdSO4 (precipitado blanco) +2HCl