
Fig.1
GRUPO HEUREMA. EDUCACIÓN SECUNDARIA
ENSEÑANZA DE LA FÍSICA Y LA QUÍMICA
PRECIPITACIÓN DE
SALES DE PLATA (III)
3.Nitrato de plata y haluros independientes
Dado que hay
sales de plata (fig.1), precipitarán con cloruro sódico (fig.2), formando AgCl ( Kps=1,8.10-10),
ahora no se desprenden burbujas de dióxido de carbono como en los casos anteriores, por el medio ácido(fig.3).

Fig.1

Fig.2
Las reacciones químicas que se producen son
Ag++NaCl ![]() AgCl (Blanco) +Na+
AgCl (Blanco) +Na+
4. Si ahora se agrega NaBr, precipitará bromuro de plata amarillo ( Kps=8,3.10-16), que por su mayor formándose algo de bromo (rojizo), que densidad irá hacia el fondo del tubo ( fig 4,5 y 6).
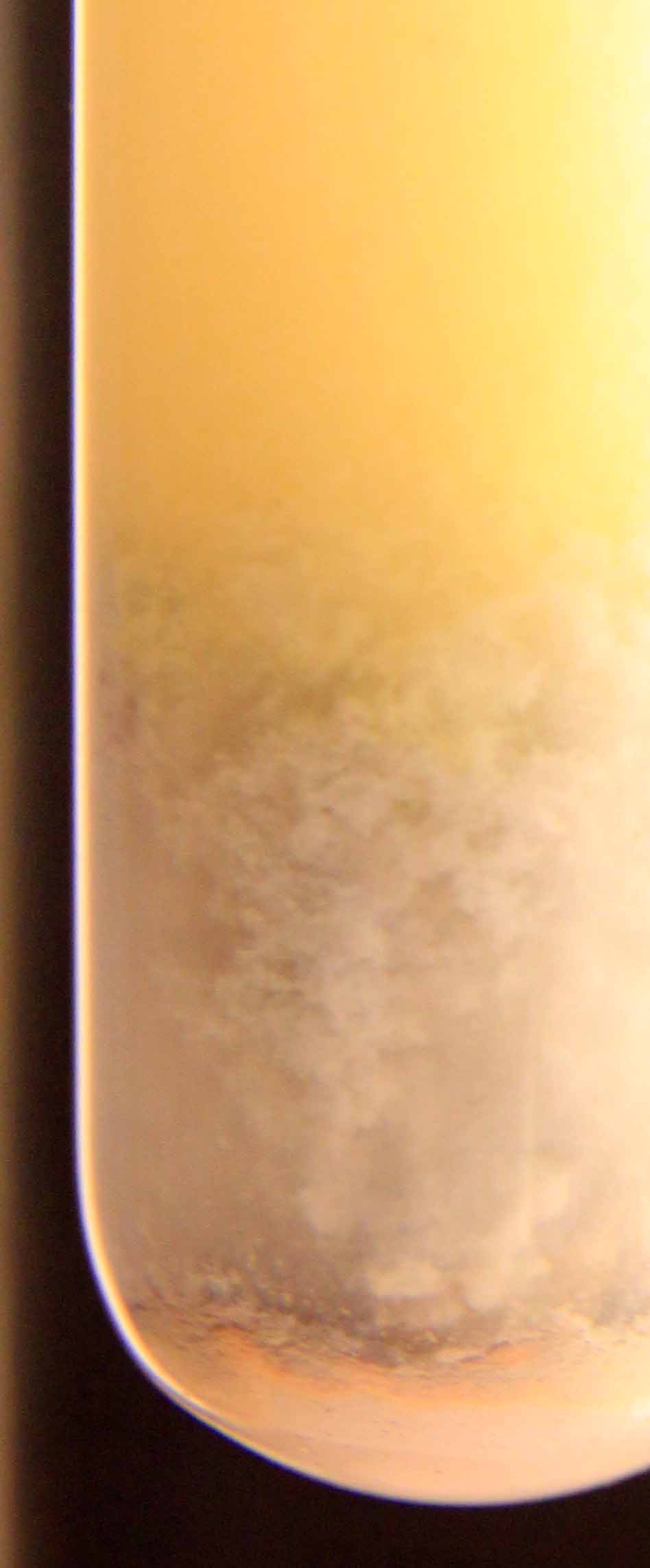
Fig.4

Fig.6(detalle)
La reacción de precipitación será:
Ag+ + NaBr ![]() AgBr +
Na+
AgBr +
Na+

Fig.5(ampliación)
5. Si ahora se agrega KI, precipitará yoduro de plata marrón (Kps=8,3.10-16), que por su mayor densidad irá hacia el fondo del tubo (fig. 7 a 10)

Fig.10
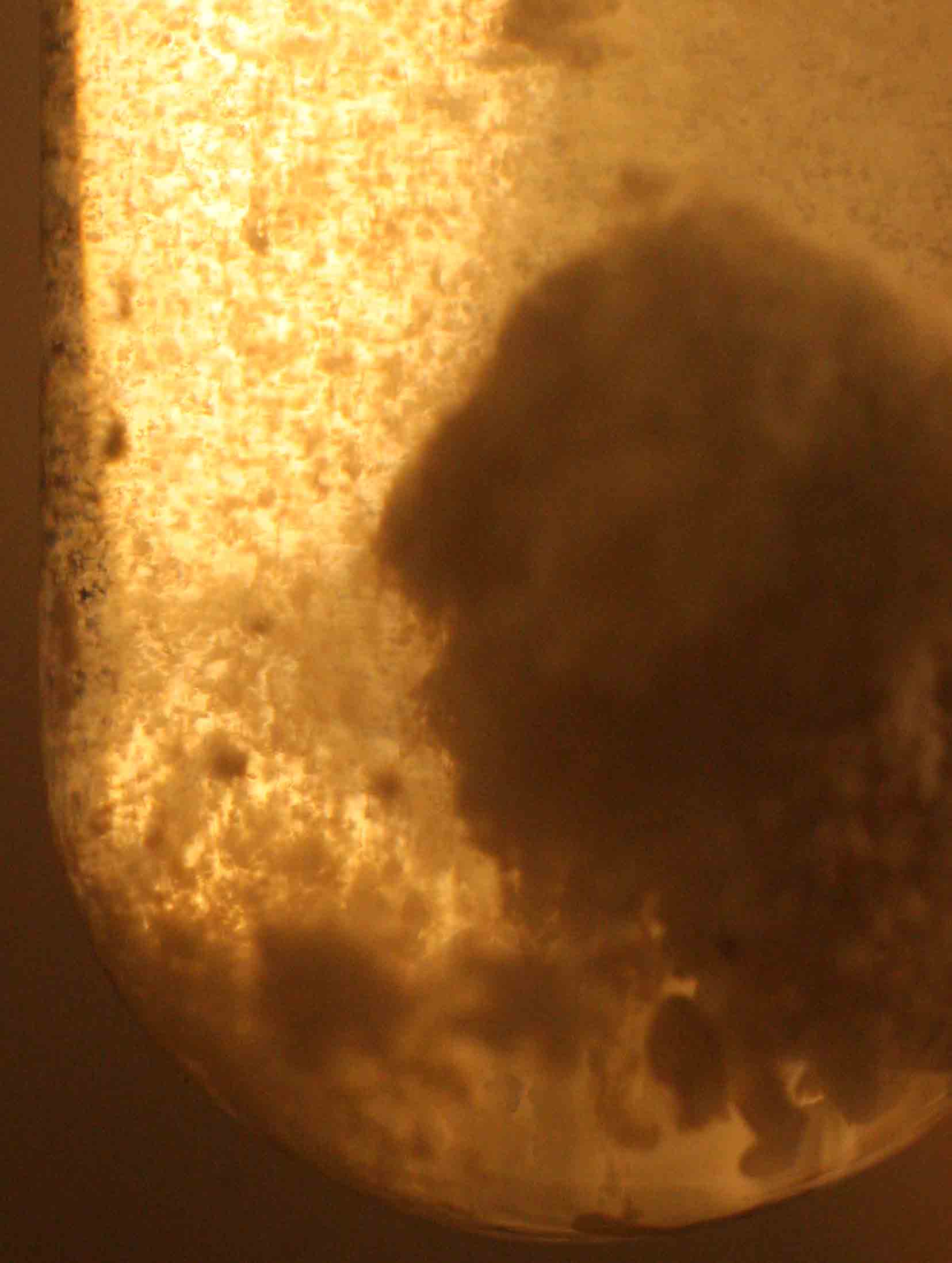
Fig.8

Fig.7

Fig.9(ampliación)
5. Con el tiempo la plata se reduce por acción de la luz, oscureciéndose (fig.10 y 11).

Fig.11 (detalle ampliado)

Fig.3
La reacción de precipitación será:
Ag+ + KI ![]() AgI +K +
AgI +K +