
Fig1
GRUPO HEUREMA. EDUCACIÓN SECUNDARIA
ENSEÑANZA DE LA FÍSICA Y LA QUÍMICA
Pilas electroquímicas con
objetos 3
Una vez obtenido el patrón plata a través una sortija, vamos
a compararlo a través del par Ag+/Ag, con diferentes objetos metálicos. Primero
frente a una moneda de plata
Para
ello se realizará el montaje que se observa en la fig1. Un vaso de precipitados
pequeño (100mL), con una disolu-ción de nitrato de plata aproximadamente 1M, en el que se sumerge una
sortija, y otro vaso de precipitados similar en el que se dispone otra disolución
de nitrato de plata también 1M, con una moneda de plata unidos ampos por un
puente de papel de filtro. Conectamos al polo positivo del voltímetro por
el cable rojo la sortija de plata,
mientras que la moneda lo hacemos al
polo negativo por el cable azul (fig.1). La diferencia de potencial tiende
a 0. Sin embargo si cambiamos la moneda de plata por otra de otro país (fig.2),
la diferencia de potencial se modifica, según el porcentaje de plata de la
aleación.. El detalle se aprecia en
la fig.3 y la pila formada se esquematiza
en la fig 4 (siempre que haya pasado cierto tiempo).

Fig1

Fig.2

Fig.3 (ampliación)
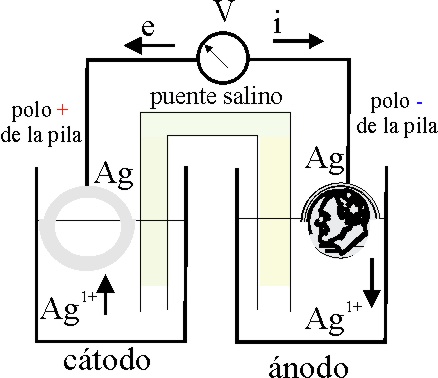
Fig.4
Teóricamente
la diferencia de potencial de la pila formada debería ser de 0,80-0,80V=0,0V,
en condiciones estándar, que no se dan en este caso, marcando 0,01 o 0,03V.según
la concentración en plata de la moneda
El proceso
redox que tendría
La pila operaría
como una pila de concentración.La simbología de la pila electroquímica formada
será la dada en la fig.6.
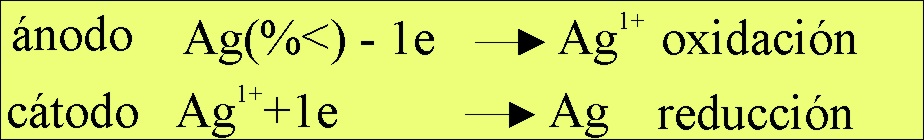
Fig.5

Fig.6
Si sustituimos la moneda de plata,
por una barra de plomo, en una disolución 1M de nitrato de plomo(II)
la pila formada se haría con dos objetos: sortija de plata/ barra de
plomo, obteniendo el resultado que se
observan en las figuras 7 , basado en el proceso dado en la Fig. 8, según
el cuál la diferencia de potencial teórica que debería marcar el voltímetro
en condiciones estándar sería de 0,799-(-0,126)V=0,925V. En nuestras condiciones
obtenemos 0,89V. El proceso y la simbología de la pila formada, vendrían en
las Fig. 9 y 10.

Fig.7

Fig.8
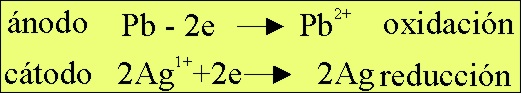
Fig.9

Fig.10