
Richter en Breslau
ENSEÑANZA DE LA FÍSICA Y LA QUÍMICA
Jeremías
Benjamín Richter, el padre de la estequiometría.
Dentro de unos
días, se cumplirá el 250 aniversario del nacimiento de Jeremías Benjamín Richter,
que lo hizo el 12 de marzo de 1762, en Hirchberg (Silesia), actualmente Jelenia
Gora en Polonia. Fue un adelantado de su tiempo, porque se empeñó en tratar
la química, matemáticamente
[1]
, lo cual a nadie se le ocurría a finales del siglo XVIII.
Es más, el nombre que propuso para la nueva ciencia; la estequiometría o el
arte de medir los elementos químicos, fue motivo de que se considerase a dicha
ciencia como muy compleja y que ningún científico de la época le prestara
atención
[2]
.
Su padre era comerciante, y el destino del hijo era convertirse en aprendiz de su tío, arquitecto e ingeniero militar. Los reveses económicos de la familia, le hicieron entrar en el servicio militar, en el cuerpo de ingenieros en Breslau, donde estuvo desde 1778 hasta 1783, y del que fue expulsado por un problema disciplinario [3] . Su formación química la hizo leyendo el diccionario de Química de Macquer. Después entró en la universidad de Könisberg, donde fue alumno de Kant, graduándose el 30 de abril de 1789, con una disertación De usu matheseos in Chemia (el uso de las matemáticas en la Química), permaneciendo durante algún tiempo como Privatdozent en dicha universidad, sin remuneración [4] . Cree que el hidrógeno (no se conocía en aquél tiempo), que se desprendía al tratar los metales con un ácido, era flogisto, tratando de determinar su peso [5] . Pero sus pocos recursos financieros no le permitieron seguir en la facultad, empleándose en 1790 como tutor en la casa del Señor de Leschwitz, sin dejar sus experimentos químicos [6] .

Richter en Breslau
En 1791 encontró que al precipitar tartrato de calcio, desde una solución de tartrato potásico tratándola con acetato de calcio, el sistema resultante es neutro, haciendo notar:que está demostrado experimentalmente que este hecho se verifica en todas las descomposiciones por doble afinidad, siempre que los compuestos usados en esas descomposiciones sean neutros. Estableciendo la siguiente conclusión: Si los componentes de dos compuestos neutros son A-a (a) y B-b (b), las relaciones de masas de los nuevos compuestos neutros establecidos en la doble descomposición son A-a/b y B-b/a.
En 1792, publica sus tres volúmenes de Angfängsgründe der Stöchyometrie (Rudimentos de estequiometría) [7] . El primer volumen Die reine Thermimetric und Phlogometrie, dedicado a las medidas calorimétricas y los otros dos Angewandte Stoichiometrie, ya dedicado a las relaciones entre las combinaciones químicas. Sin embargo no se encontraba a gusto con su trabajo de tutoría, haciendo diversas solicitudes para un puesto docente.
En enero de
1795, consigue un trabajo en la oficina minera de Silesia, en Breslau. En
él tenía que analizar minerales, y relatando sus características. Su sueldo
anual era de 300 thalers
[8]
. Tenía un asistente, con el que compartía una habitación
llena de humedad que oxidaba sus instrumentos de análisis. Su trabajo resultó
ser bien considerado, por lo que se le subió el salario a 400 thalers al año
siguiente.
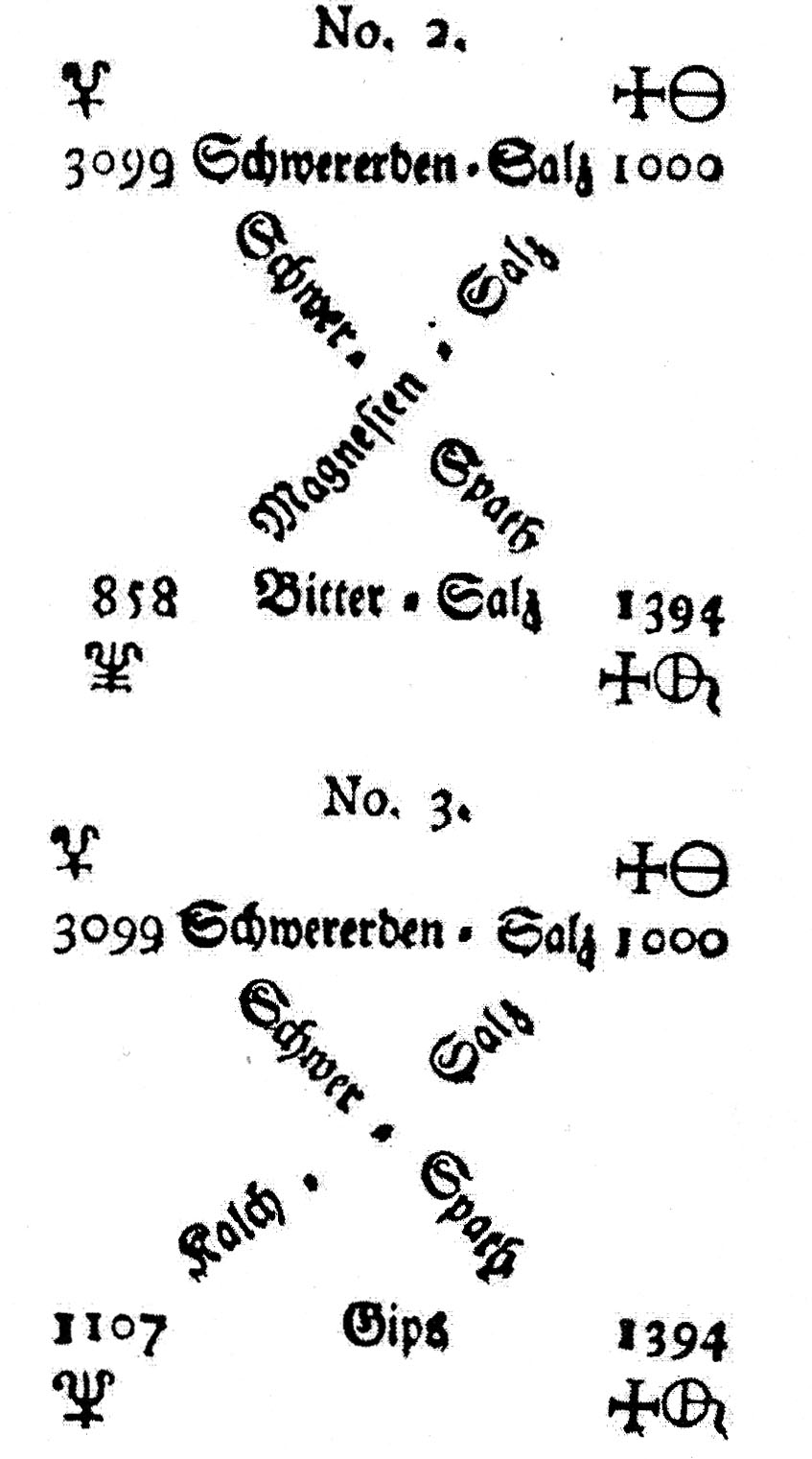
Fig.1
En 1795, en
las aclaraciones a su tratado de estequiometría, publica lo que sería después
la ley de las proporciones recíprocas, en estos términos: Si P es la masa de un elemento determinante y a,b,c,d, las masas de los
elementos por él determinados y si Q es la masa de otro elemento determinante,
y ",$,(
y *,
las masas de los elementos por él determinados, y de modo tal que a y ",
b y $,
c y (,
d y *,
representen las masas del mismo elemento
y si las masas de compuestos neutros P+a y Q+$, P + a y Q+(,
etc. se descomponen por doble afinidad de
que modo que los productos resultantes sean neutros, se verifica que las masas,
a,b,c y d tienen entre sí relaciones cuantitativas iguales a las correspondientes
masas ",$,(
y *,
o inversamente
La parte experimental, se hizo con medidas a partir de la reacción BaCl2 + MgSO4 = BaSO4 [9] + MgCl2, cuya exposición original se presenta en la fig.1 [10] . Los números al margen corresponden a las partes de cada sustancia, que reaccionaban con partes de la otra. Así 3099 Schwererden saltz (sal de tierra pesada) [11] 1000, implicaba que la relación entre óxido y ácido en esta sal era de 3099/1000. Mientras que 1000 partes de ácido clorhídrico, neutralizaban 858 partes de magnesia, y 1000 partes de ácido sulfúrico, 616 de magnesia (MgO), por lo tanto la neutralización de 858 partes de magnesia, necesitarían 1394 partes de ácido sulfúrico. Igualmente estudia las relaciones en la reacción: BaCl2 + CaSO4 = BaSO4 + CaCl2 parte inferior de la fig1. De esa forma calculó los pesos equivalentes, que llamó Massenzahlen de 18 ácidos y 30 bases. El problema de esta tabla era que sus pesos equivalentes no se referían a una base común [12] .
Sus mediciones de los pesos de los metales que se disolvían en pesos fijos de ácidos le llevaron a deducir la afirmación de que los pesos de distintas bases que saturan un peso constante de ácido, contienen el mismo peso de oxígeno para el mantenimiento de la neutralidad. Sin embargo obsesionado con las matemáticas [13] creía que los pesos de combinación de los ácidos estaban en progresión geométrica, mientras que los de las bases lo hacían en progresión aritmética.
En 1798, al morir Beyling, segundo químico (segundo arcanista) [14] de la Real fábrica de porcelana, se le ofrece el puesto a Richter, con un sueldo de 500 thalers, pero él pide 700, porque tiene que trasladarse a Berlín, lo cual se le concede.
En abril de
1801, fue nombrado asesor de la minería, con un sobresueldo anual de 250 thalers.
Nunca se casó, y toda su vida se la pasó trabajando e investigando en las
condiciones más precarias.

Richter en Berlín
Sus investigaciones
no se ciñeron únicamente a la estequiometría. Para conseguir dinero en sus
épocas de penuria, construyó higrómetros y areómetros para líquidos (excepto
del mercurio) que ofrecía por 10 thalers, incluso alcoholímetros a 4 thalers.
Fue el primero en usar el cloruro de calcio para preparar alcohol absoluto. Por estas fechas,
publicó una tabla de densidades para la mezcla alcohol-agua, que se usó por
aquella época con el nombre de escala de Richter
[15]
, así como otra tabla de densidades de disoluciones acuosas de ácidos y bases.
Aplicando sus métodos matemáticos encontró una serie de relaciones regulares entre los pesos de combinación de algunos elementos, que le permitieron ordenar los metales alcalinos y alcalinotérreos en una serie aritmética, precursora de todos los sistemas periódicos [16] .
En el laboratorio de la Real Fábrica de porcelana elaboró un método para separar el cobalto y el níquel, y se especializó en la preparación de soluciones coloidales para teñir las porcelanas, tal como el oro coloidal [17] .
Sus últimos años se dedicó a los procesos metalúrgicos y en 1806 publica un tratado sobre licuación.
El 4 de abril de 1807, muere de tuberculosis en Berlín a los 45 años recién cumplidos.
Firma de Richter
[1] Para él la Química era una rama de las matemáticas, influenciado por su maestro Kant, que había establecido que .En las ciencias de la naturaleza sólo se encuentra la ciencia auténtica lo que contiene de Matemática.
[2] Hasta hace poco tiempo la copia de la primera edición de sus volúmenes, en la biblioteca nacional húngara, en Budapest, permanecía con las hojas pegadas (nadie se había interesado por la obra, ni se habían abierto las hojas). Pero para Richter, como confesaría mas tarde, era la palabra mejor y más corta que podía expresar las relaciones cuantitativas en la Química, compuesta por los términos griegos stoicheion (fundamental, elemental, indivisible), y metrein (medida).
[3] Por lo visto su nombre había desaparecido, por lo menos 15 veces de las listas, cuando se pasaban.
[4] Los primeros detalles de su vida se deben a Carl Löwig, en 1874, y posteriormente a Moufang, director de la Real fábrica de porcelana en Berlín.
[5] Escribiría en 1792:Parece ser que el flogisto, con combinaba con la materia, incendiándola produciendo lo que llamamos luz. Era normal porque en su época estaba en plena vigencia la teoría flogística.
[6] Para poder hacer investigación, con sus pocos recursos, aumentados con trabajos extra como la medición de fincas, equipó un pequeño laboratorio, donde trabajaba. Sin embargo nunca se consideró un manipulador y analista químico hábil. Siempre perdía algo de sustancia al tratarla, por eso decía que necesitaba partir de 500granos y no de 100.
[7] Este libro fue mal acogido e interpretado, por ello necesitó aclararlo en las 11 secciones de su Über die neuern Gegenstande de Chemie, (Acerca de los nuevos temas de Química), escritas desde 1793 a 1802. A un crítico que declaró no entender las relaciones en las neutralizaciones le respondió:La naturaleza sería realmente pobre si se limitara a lo que podría ser entendido por mi y mis críticos.
[8] El thaler, moneda de plata, precursor etimológico del dólar, equivalía aproximadamente a 0,75 dólares.
[9] El sulfato de bario era el espato pesado, por la forma de cristalizar y por contener bario.
[10] Como se aprecia empleaba la notación simbólica de aquella época (para mas detalles ver en esta web, DFQ13). Se debe tener en cuenta que el ácido clorhídrico era ácido de sal marina y tenía oxígeno y el ácido sulfúrico era el óleo de vitriolo y era SO3).
[11] La tierra pesada o baroto, era el óxido de bario, que recibe este nombre precisamente por ser mas pesada que otras cales(óxidos), baros es pesado en griego.
[12] Eso lo hizo Bertollet, con los datos de Richter, 6 años después, tomando como 100, al sulfúrico.
[13] Los 11 tomos que escribió desde 1795 a 1802, Acerca de los nuevos temas de Química, llevaban como lema las palabras del bíblico libro de la sabiduría:Todo ha sido ordenado por Dios según medida, número y peso.
[14] Todos los sistemas empleados en confeccionar las porcelanas de la Real Fábrica, así como los pigmentos que las decoraban eran secretos.
[15] Nada que ver con la escala de intensidad sísmica, creada en 1935 por Charles Richter.
[16] Sin embargo incurrió en el error de considerar como elemento químico la llamada tierra de Agust, descubierta por Trommsdorff, que no sería otra cosa que fosfato de calcio.
[17] Sólo 100 años después serían apreciados sus descubrimientos, cuando llamaron la atención de Ostwald.