ENSEÑANZA DE LA FÍSICA Y LA QUÍMICA
TEST DE QUÍMICA 69. ORGÁNICA 9.ISOMERÍA ÓPTICA Y GEOMÉTRICA
10.161. Isomería óptica en ciclos
Los ciclos planos aun los mas sencillas, pueden tener isómeros ópticos basta con
dispongan de sustituyentes, que provoquen la asimetría molecular así de los
compuestos dados
:1) dimetilciclopropano; 2) clorometilciclopropano
3) diclorociclopropano; 4) ciclopropano
Dirás que sólo tendría isomería
óptica a) el 1 b) el 2 c) el 3 d) el 4
10.162*. Para que un ciclo alcano plano con número impar
de carbonos tenga isomería óptica hace falta que:
a) No tenga plano de simetría
b)Tenga por lo menos un hidrógeno sustituido
c)Tenga los dos hidrógenos vecinales o alternos con
sustituyentes diferentes
d)Tenga los dos hidrógeno de un carbono con sustituyentes
diferentes
10.163*.No hace falta tener carbonos asimétricos para
posee isomería óptica, basta que la asimetría molecular, y eso ocurre por
varias circunstancias, fundamentalmente por una configuración capaz de crear una imagen especular, como ocurre en el
caso de los alenos, compuestos con dos dobles enlaces
acumulados. Esta asimetría descubierta por Vant’Hoff en 1875, no fue investigada hasta 1935, en sus derivados tal como el 2,3-pentadieno y se debe a que:
a) El carbono central de los dobles enlaces acumulados
tiene una hibridación sp y no sp2
b)Toda la molécula de un aleno está en el mismo plano
c) La nube pi de los dobles enlaces está en diferentes
plano perpendiculares
d) Los sustituyentes de los carbonos 2 y 4 son distintos.
10.164. Un alqueno con dos dobles enlaces necesita para su combustión completa 7 veces su volumen
de oxígeno. El único compuesto con estas características y con isomería óptica
será el
a) 1,3-butadieno b) 2,3-pentadieno c)1,4-pentadieno c)2,3-butadieno
10.165. Otros compuestos sin carbono asimétrico que sin
embargo pueden tener asimetría molecular son los espiranos.
Esto es debido a que los ciclos:
a) Que tienen un
solo carbono en común están en diferentes planos
b) Arrancan según
una disposición tetraédrica
c) Se disponen
linealmente
d)Están en el mismo plano
10.166. El espirano mas
sencillo con isomería óptica deberá ser el:
a) espiro(2,2)butano b)1-metilespiro(2,2)pentano
c)1,2-dimetilespiro(2,2)pentano d)1,4-dimetilespiro(2,2)pentano
10.167*. Todavía pueden existir entre los hidrocarburos, compuestos
con actividad óptica sin carbono asimétrico, simplemente por impedimento
estérico que no les permita convertirse por giro a través de enlaces sigma,
provocando que tengan que existir en planos diferentes, esto ocurre en:
a) ciclos con disposición espacial que implique asimetría
molecular
b) ciclos aislados con carbonos asimétricos
c) ciclos condensados sin planos de simetría
d)biciclos con sustituyentes orto voluminosos
10.169.Van’t Hoff, separó
ambas isomerías, la óptica y la geométrica, especificándolas. Al principio
estos últimos isómeros se denominaron maleoideo (como el ácido maleico)
y fumaroideo (como el ácido fumárico),
hasta que 17 años después, Baeyer introdujo el término de isomería cis-trans(cis,
latín; a ese lado, trans, latín; al otro lado). De
esa forma el ácido anteriormente dibujado por Wislicenus sería un isómero:
a) Cis b) Trans c)No tendría isomería geométrica d)No tendría dobles enlaces
10.170*.La clave para dos compuestos tengan isomería
geométrica, es que posean un plano de irrotacionalidad,
y sustituyentes diferentes en ambos planos. Esto puede ocurrir de entre los
compuestos dados de fórmula molecular C5H10:
1) 2-metil-1-buteno 2)
2-penteno 3)
1,2-dimetilciclopropano 4)
1,1-dimetilciclopropano
en el : a) 1 y 4 b)2 y 4 c)2 y 3 d)1
y 4
10.171*. No solo los compuestos con doble
enlace poseen un plano de irrotacionalidad, esta
situación puede ocurrir en:
a) Cualquier tipo de compuesto cíclico
b) Ciclos con sustituyentes diferentes
c) Compuestos que no puedan rotar por
impedimento estérico
d) Compuestos con triple enlace
10.172. Posteriormente, los trabajos de Kahn, Ingold y Prelog, al fijar en 1956, las reglas secuenciales para la
denominación de estereoisómeros, con cuatro
sustituyentes diferentes en los carbonos con doble enlace, el cis, será seqcis (secuencia cis), o Z(del
alemán zusammen, juntos) y el trans,
será seqtrans, o E(del
alemán entgegen, opuestos). Según eso el número de
isómeros trans con fórmula molecular C5H10 será: a) 2 b)5 c)3 d)4
10.173. Cuando los 4 grupos o átomos a ambos lados del plano de irrotacionalidad son
diferentes, el convenio para proponer un isómero cis o Z, sería:
a) Del mismo lado los de mayor masa atómica
b)Del mismo lado los de mayor número
atómico
c)En lados diferentes según el número
atómico
d)En lados diferentes según su peso
atómico
174. El menor hidrocarburo saturado que posee isomería geométrica será el:
a) 1,1-dimetilciclopropano b)metilciclopropano
c) 1,2-dimetilciclobutano d)1,2-dimetilciclopropano
10.175. De todos los derivados diclorados de un
hidrocarburo saturado de 3 carbonos que posean isomería geométrica solo podrá
ser posible en el:
a) 1,2-dicloropropeno b)1,1-diclorociclopropano
c) 1,1-diclorociclopropeno d) 1,2-diclorociclopropano
10.176. Los hidrocarburos saturados de fórmula C6H12, que
tienen isomería geométrica serán:
a)1,2-dimetilciclobutano b) 1,1-dimetilciclobutano
c)metilciclopentano d)
1,2,3-trimetilciclopropano
10.177. El ácido monocarboxílico de menor peso molecular que presente isomería geométrica, será el ácido:
a)2-metilciclopropilmetanoico b)3-butenoico
c)3-metilciclopropilmetanoico d)2-butenoico
10.178.Un compuesto orgánico cíclico presenta la siguiente composición:
C=69,77%- H=11,63% - O=18,60%. Si tomas 2 g. del mismo y lo calientas hasta
27ºC ocupa en fase gaseosa a 700mmHg . de presión 0,621L si presenta isomería
geométrica . Con estos datos dirás que el único compuesto que la presenta será el:
a) 1-metilciclobutanol b)2-metilciclobutanol
c) 3-buten-2-ol d)
2-buten-2-ol
Datos: C=12; H=1; O=16.R=0,082atm.L.K-1.mol-1
10.179. Dispones de un compuesto orgánico cíclico de
C,H y O del que sabes que contienen un 54,55% de carbono y un 36,36% de
oxígeno. Además 2g del mismo disueltos en 100mL de agua producen una disolución
que congela a -0,42ºC, a presión normal, si sabes que posee isomería geométrica,
dirás que el único compuesto con esas características es el
a) 3-butenoico b) 2,3-ciclobutanodiol
c) 2-buteno-2,3-diol d)
1,1-ciclobutanodiol
DATOS : MASAS ATÓMICAS: C,12- H,1-O,16. Constante crioscópica del agua =1,86 K.kg.mol-1

10.168*. Wislicenus, también
justificará la isomería geométrica, término creado por él, que incluía también
la isomería óptica, para explicar el comportamiento de los ácidos fumárico y maleico, como se ve,
este último en el dibujo, con un doble enlace en la arista común de los dos
tetraedros, esta isomería geométrica era debida a:
a) La interconversión de los dos isómeros implicaba la rotura del enlace
b) No era posible girar a través de una arista
c)Tenían propiedades diferentes
d)Uno era imagen especular del otro
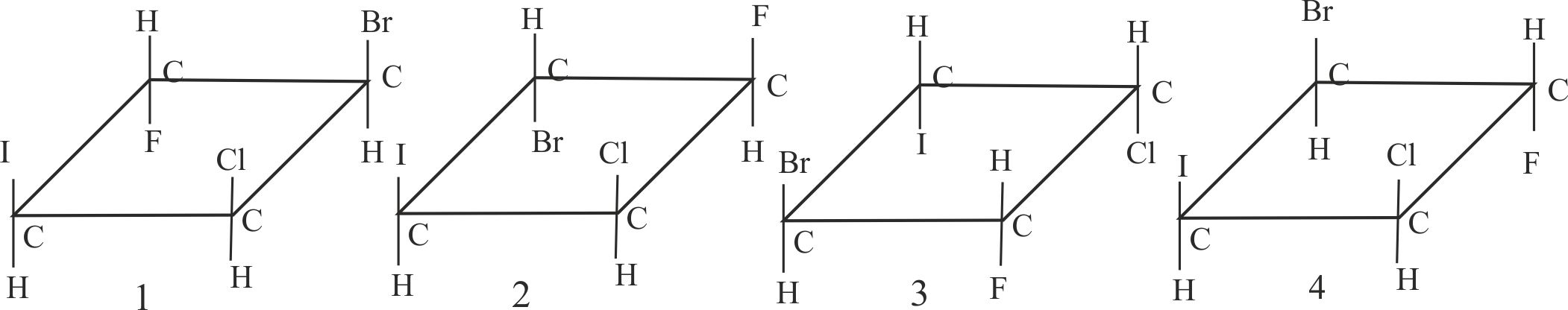
10.180. De los compuestos dados serán
isómeros cis:
a) el 1 y el 2 b) El 2 y el 3 c)
el 1 y el 4 d) el 2 y el4