
Fig.1
ENSEÑANZA DE LA FÍSICA Y LA QUÍMICA
DICROMATO POTÁSICO Y MONEDAS I
Siguiendo la reacción de monedas españolas con oxidantes, ahora veremos
la acción del dicromato potásico
1.Dicromato potásico
diluido y moneda española de una peseta de peseta de 1985
(Composición 1,2g de Al)
Trabajando como en prácticas anteriores, con una gota de K2Cr2O7 (fig.1), reacciona lentamente por sus bordes(fig.2-5),; después sobre la cara, destruyéndose el relieve en la cara sumergida en el oxidante (Fig.6). Al agregar una gota de ácido clorhídrico diluido para activar el oxidante, el metal reacciona violentamente (fig.7-11), por desprendimiento de hidrógeno, produciéndose sal de cromo (III) verdosa.

Fig.1

Fig.2

Fig.3

Fig.5

Fig.4

Fig.6
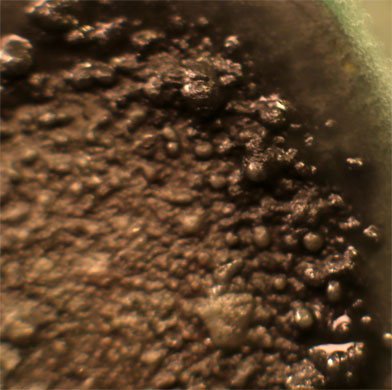
Fig.9 (detalle)
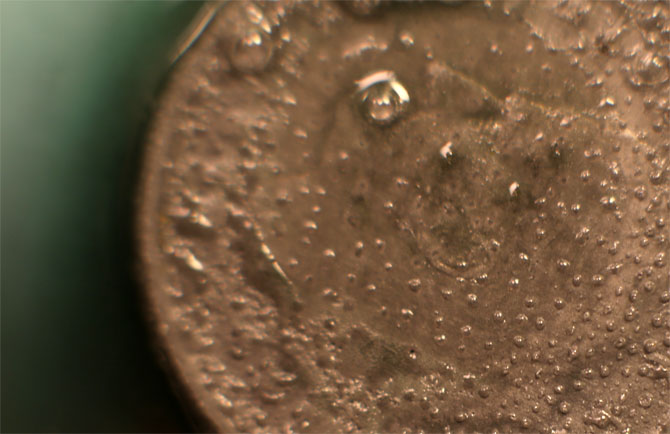
Fig.7
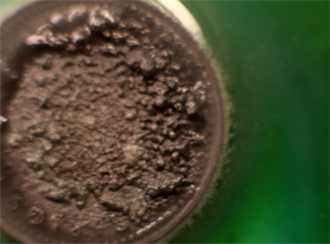
Fig.8

Fig.10
REDUCC 6HCl+6e- = 3H2+6Cl-
OXIDAC: 2Al - 6e =
2Al3+
___________________________________
6HCl+2Al= 2AlCl3+ 3H2
Los dos procesos redox que tienen lugar son:
REDUCC: K2Cr2O7 + +14HCl+6e- = 2Cr3++2K++14H+ +7O2-+14Cl-
OXIDAC: 2Al - 6e = 2Al3+
________________________________________________
K2Cr2O7 +2Cu= 2AlCl3+ 7H2O+
2CrCl3 +2KCl
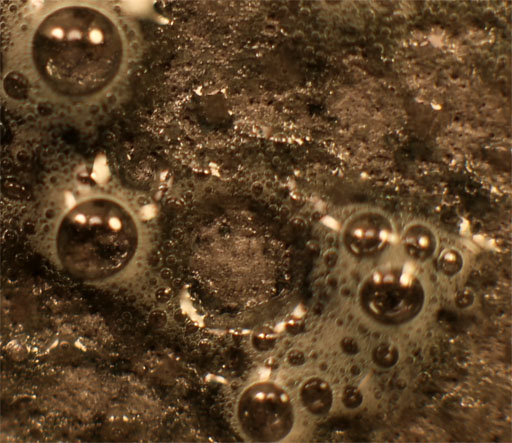
Fig.11( detalle)