
Fig.1
ENSEÑANZA DE LA FÍSICA Y LA QUÍMICA
ÁCIDO ORTOFOSFÓRICO
Y METALES (II): Actuando sobre
magnesio
1.Ácido ortofosfórico
14M y cinta de magnesio
Trabajando como en prácticas anteriores,
con una gota de ácido ortofosfórico 14M(fig.1), que reacciona desde el inicio violentamente (fig.
2), atacándo la cinta de magnesio, con desprendimiento de hidrógeno de forma
espectacular (fig.3-4) ( hasta el punto de desenfocar la imagen), partiéndose
la cinta en varios fragmentos(fig.5-10), hasta prácticamente desparecer el
magnesio (fig 13-16), formándose ortofosfato de magnesio insoluble y también dihidrógeno ortofosfato de magnesio,
muy soluble.

Fig.1
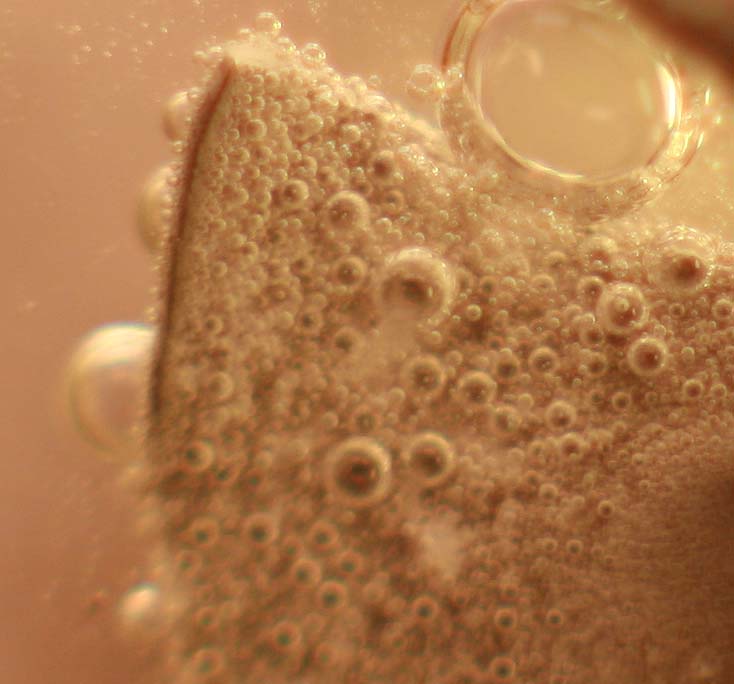
Fig 2(detalle)
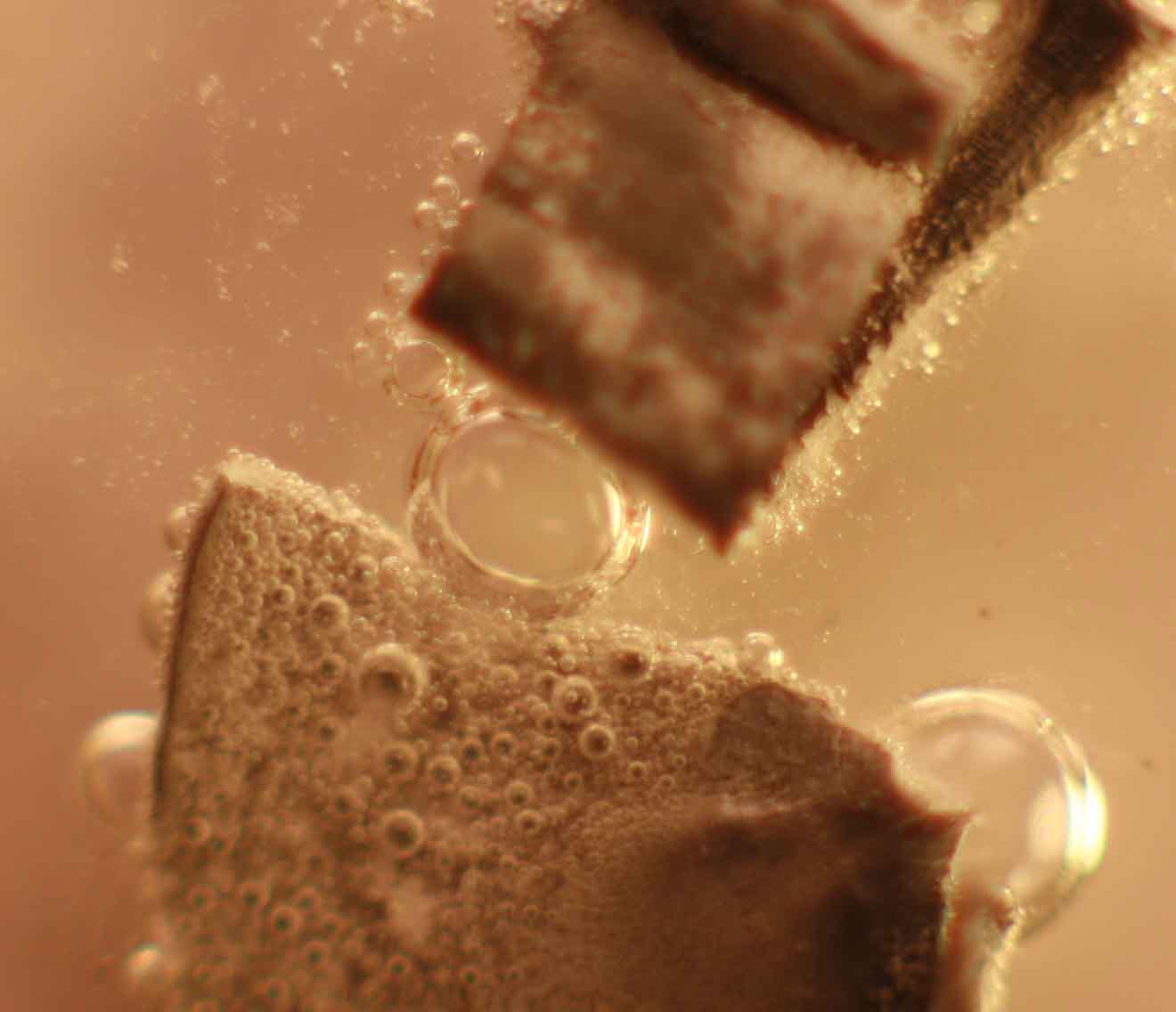
Fig.3
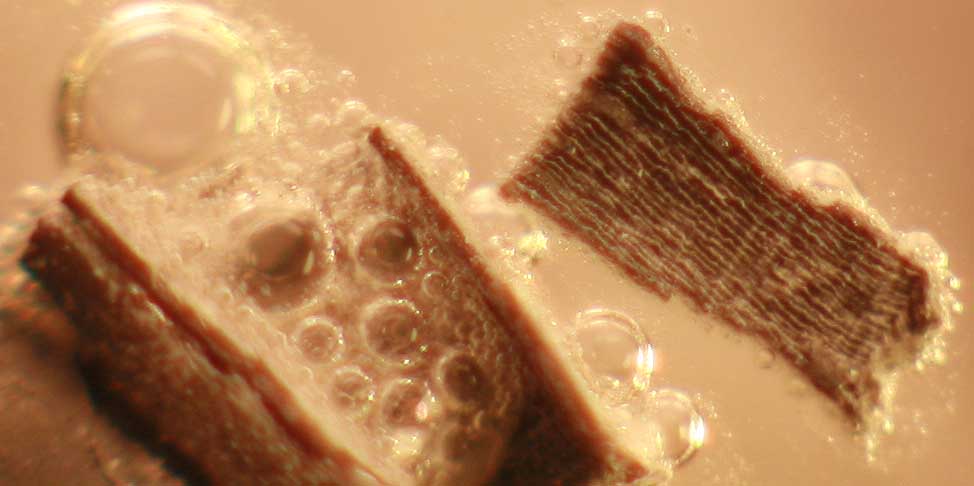
Fig.4

Fig.5

Fig.6 (detalle)

Fig.7

Fig.8 (ampliación)

Fig.9
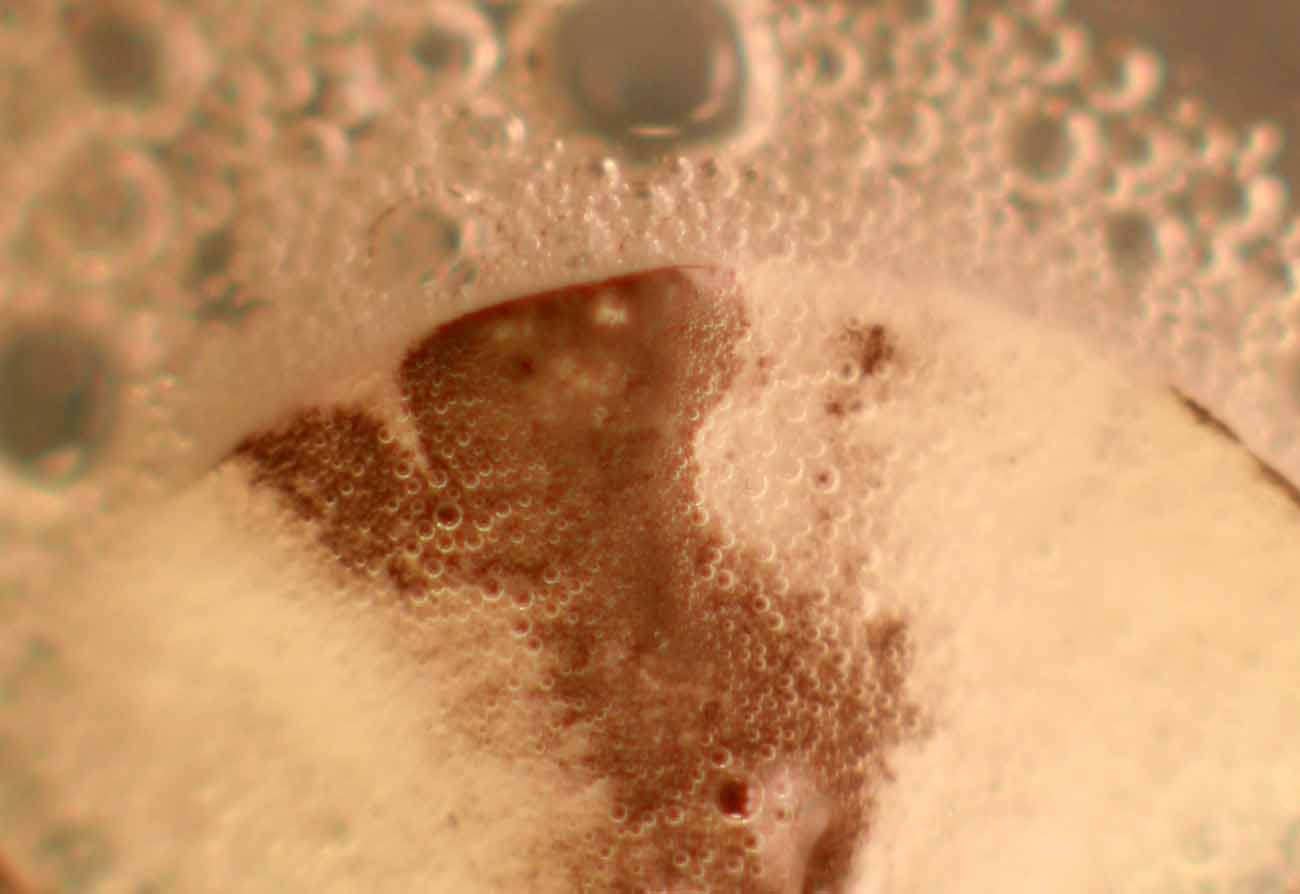
Fig.10(detalle)
Fig11 (detalle)
Fig.12 (detalle)
Las reacciones químicas que se producen son redox
La general produce ortofosfato de magnesio insoluble
REDUCC: 2H3PO4 + 6e- =
3H2 + 2PO4 3-
OXIDAC: 3Mg - 6e =
3Mg2+
______________________________________________
2H3PO4
+3Mg = 3H2(gas)+ Mg3(PO4)2
también puede producirse el dihidrógeno ortofosfato
soluble
REDUCC: 4H3PO4 + 4e- =
2H2 + 4H2PO4 1-
OXIDAC: 2Mg - 4e =
2Mg2+
______________________________________________
4H3PO4 +2Mg=
2H2(gas)+ 2Mg(H2PO4)2

Fig.13

Fig.14(detalle)

Fig.15(detalle)
Fig.16(detalle)