
Fig.1
ENSEÑANZA DE LA FÍSICA Y LA QUÍMICA
ÁCIDO CLORHÍDRICO
Y CINC
1.Ácido clorhídrico
1,13M y granallas de cinc
Se opera como en prácticas anteriores, con unas granallas de cinc, y una gota de ácido clorhídrico 1,13M (fig.1). en una superficie de 2cm2 . En este caso la reacción es muy bastante fuerte, burbujeando desde el primer momento, desprendiendo hidrógeno (fig.2 y.3). Las buerbujas son tan fuertes que desenfocan la foto (fig 4 y 5 ). La reacción se debilita al cabo de media hora (fig 6 y 7).
El proceso principal
que tiene lugar en las fotografías es el siguiente:
REDUCC:
2HCl + 2e- =
H2(g) + 2Cl 1-
OXIDAC: Zn - 2e =
Zn2+
______________________________________________
2HCl +Zn= H2(gas)+
ZnCl2
Las fotografías del proceso son las siguientes:

Fig.1
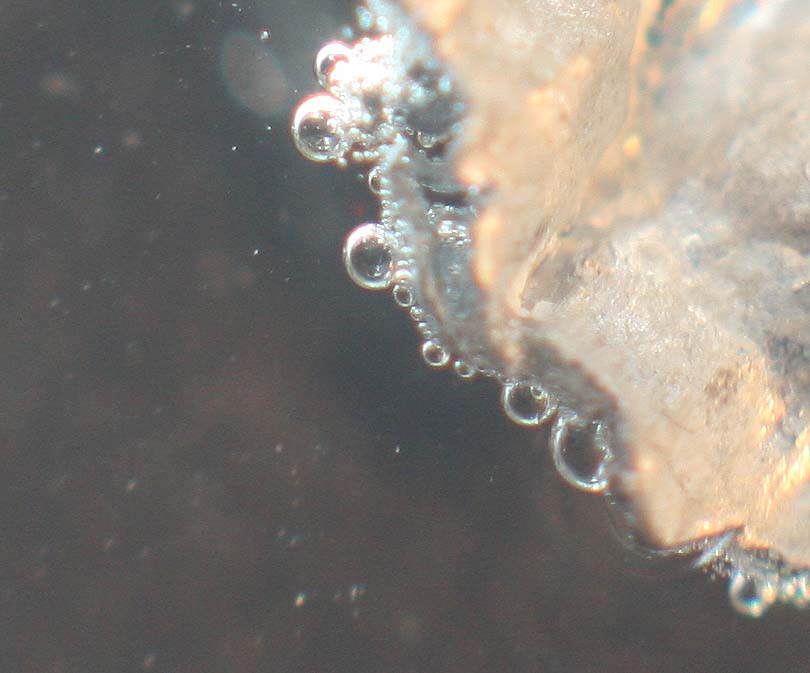
Fig.2

Fig.3

Fig.4

Fig.5

Fig.6

Fig.7 (detalle)
2. Ácido clorhídrico
11,3M + cinc en granallas
Se opera como en el caso anterior
(fig.8). En este caso la reacción es similar a la anterior pero mucho mucho más violenta, hasta el punto de
que los gases desprendidos desenfocan completamente la imagen. (fig.9). El desprendimiento
de hidrógeno produce enormes burbujas (fig. 10 y11). Al cabo de 15 minutos
la reacción toma es aspecto indicado en la fig 12.

Fig.8

Fig.9
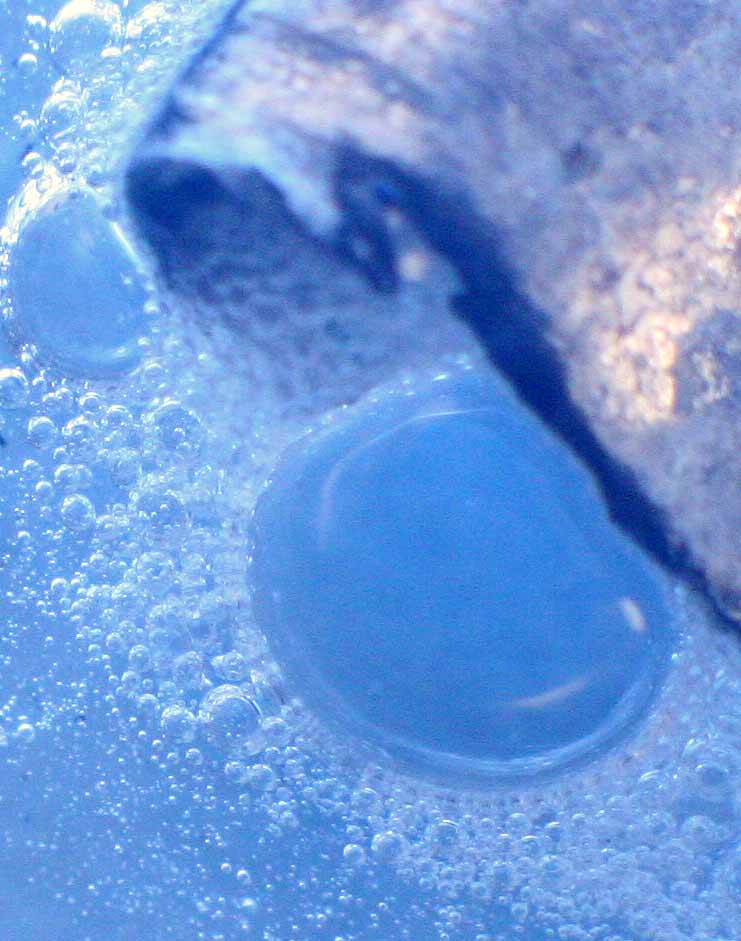
Fig.10

Fig.11

Fig.12