
Fig.2 (detalle)
ENSEÑANZA DE LA FÍSICA Y LA QUÍMICA
Ácido sulfúrico y
plomo
1. Con ácido sulfúrico
9M
Se opera como en prácticas anteriores, con granalla de
plomo, y una gota de ácido sulfúrico concentrado (fig.1 y 2). Si se recuerda,
estas mismas granallas casi no reaccionaban con el ácido nítrico concentrado
(QG43). En este caso la reacción es
inmediata, burbujeando los gases desprendidos
instantáneamente (fig.3). Después se desarrolla violentamente (fig. 4 y 5),
cesando al cabo de media hora (fig.6).A parte del proceso normal, tal como
el que tenía lugar entre el ácido sulfúrico y el magnesio (QG47), también
pueden ocurrir otros procesos, por eso se aprecian varios tipos de burbujas
diferentes.
El proceso principal
que tiene lugar en las fotografías es el siguiente:
REDUCC: H2SO4
+ 2e- = SO4 2-+
H2
OXIDAC: Pb - 2e =
Pb2+
_____________________________________________
H2SO4
+Pb = H2(gas)+
FeSO4
Proceso secundario
REDUCC:
2H2SO4 +
2e- = SO2 (g)+ 2H2O
+ SO4 2-
OXIDAC: Pb - 2e =
Pb2+
______________________________________________
2H2SO4
+Pb = SO2(gas)+ PbSO4+ 2H2O
Incluso el hidrógeno naciente reduce al ácido sulfúrico en otro proceso
secundario
REDUCC: H2SO4 + 2e- = SO2 (g)+ H2O + O2-
OXIDAC: H2 - 2e =
2H+
______________________________________________
H2SO4
+H2 = SO2(gas)+ 2H2O

Fig.2 (detalle)
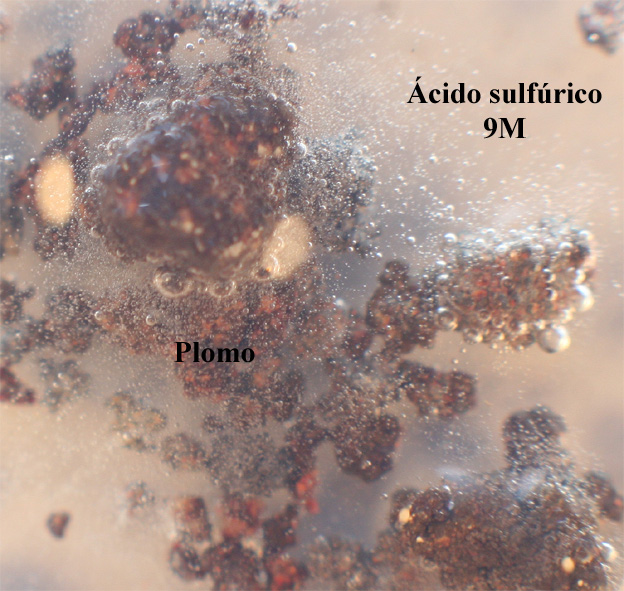
Fig.1

Fig.3

Fig.4

Fig.5 (detalle)

Fig.6
2. Ácido sulfúrico
1,5M + Pb
Prácticamente no reacciona (fig.7). Al cabo de cierto tiempo
se observan al ampliar la foto, burbujas
de hidrógeno sobre las granallas de plomo (fig.8-9)

Fig.7

Fig.8

Fig.9 (detalle)