Foto 1
ENSEÑANZA DE LA FÍSICA Y LA QUÍMICA
Oxidación de tartratos 2
Actuación redox del Co2+ como catalizador.
Se van a interpretar
una serie de fenómenos secundarios que ocurren en la doble descomposición
redox, del tartrato y del peróxido de hidrógeno(10%),
en presencia de una gota de cloruro de hexaacuocobalto(II). Para ello se disponen
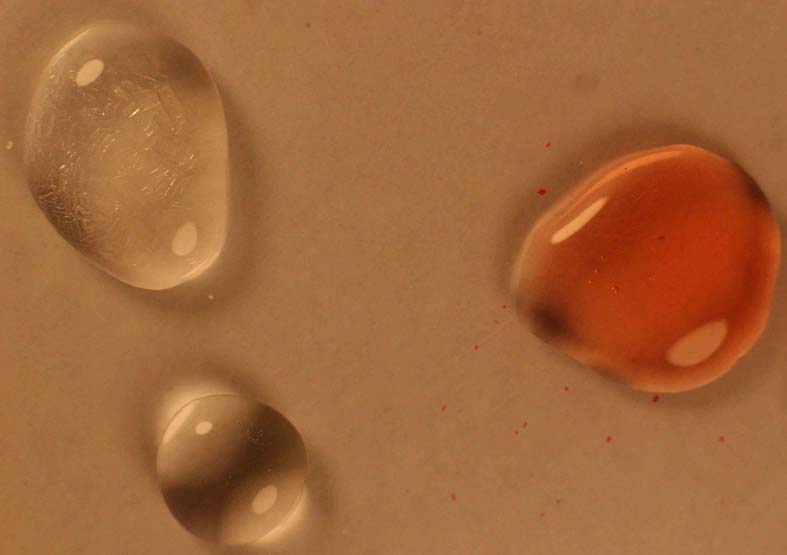
como se costumbre, 3 gotas, en una caja petri, tal como se aprecia en la foto
1
En la
gota de sal de Rochelle (tartrato sódico potásico), se pueden observar los
cristalitos de la sal), los iones complejos de hexa-acuocobalto(II), son de color rosáceo

Foto 1

Foto 2
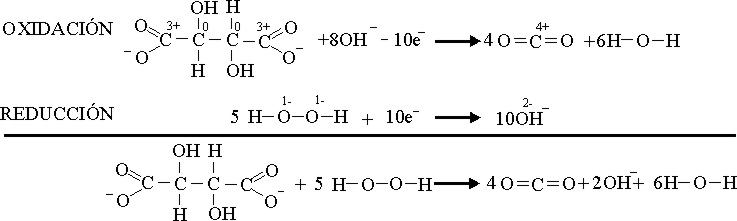
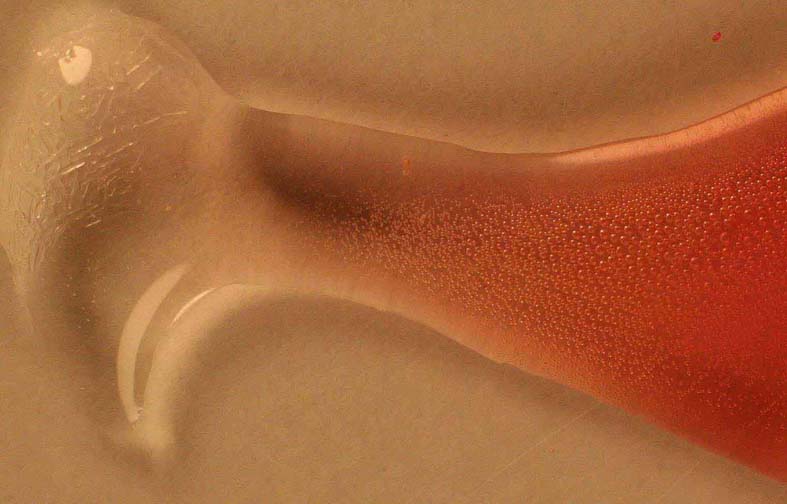
Foto 3
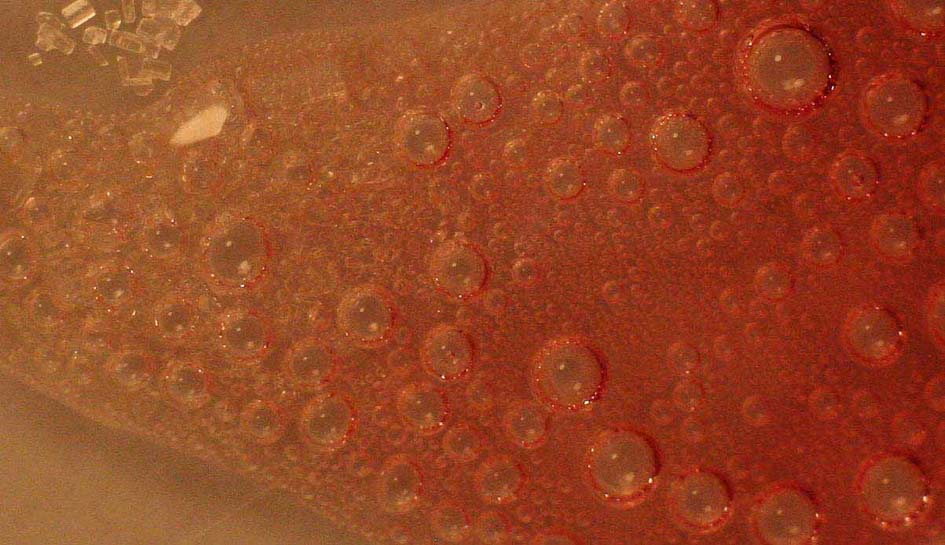
Foto 4
Pero
el Co2+, no sólo actúa como catalizador, aumentando la velocidad
con que se producen las burbujas de gas, sino que forma con el tartrato un
complejo, de color verdoso claro, que se aprecia en el extremo de la gota
(foto 5)
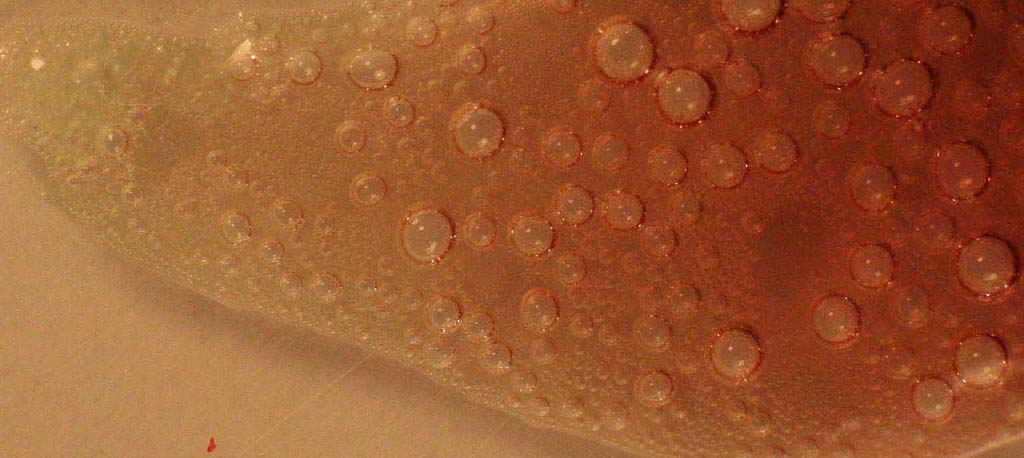
Foto 5
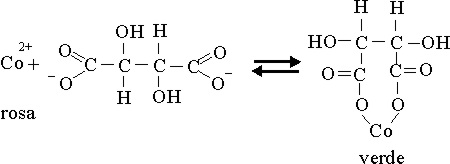
Pero también y simultáneamente
tiene lugar el proceso de descomposición del peróxido de hidrógeno, con producción
de oxígeno, tal como se aprecia en las fotos 5 y
6, con dos tipos de burbujas gaseosas, las debidas al CO2
y las ocasionadas por el O2
Detalle del proceso
(foto 6)
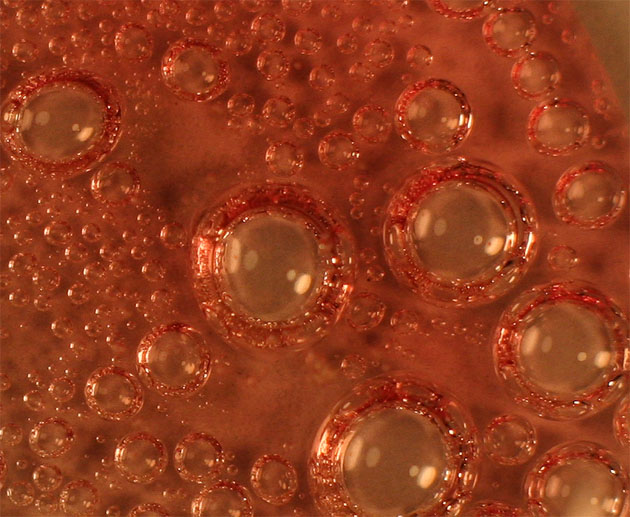
Foto 6
Al agregarle más cantidad de agua oxigenada, el cobalto(II), se oxida a cobalto(III), verde oscuro, según el posible proceso:
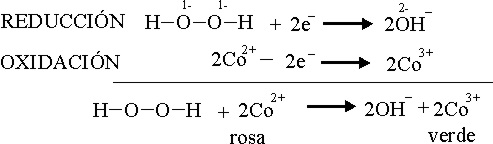

Foto 7

Foto 8
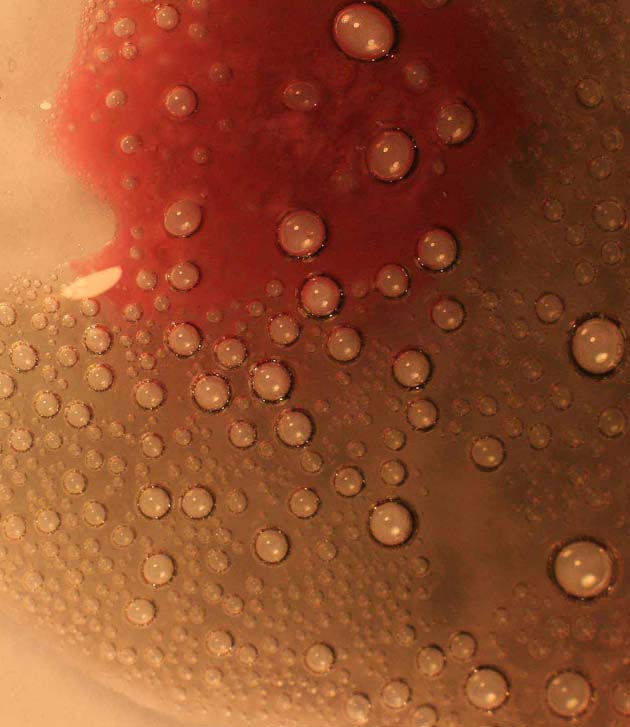
Foto 9
En la
foto 9, se agrega una gota de cloruro de cobalto(II), de esta forma se aprecia
la diferencia de colores.
Si partimos
de nitrato de cobalto(II), como catalizador, el oscurecimiento por oxidación
se aprecia rápidamente (fotos 10 y 11)

Foto 10

Foto 11