
Fig.10
ENSEÑANZA DE LA FÍSICA Y LA QUÍMICA
PRECIPITACIÓN DE SALES DE Ag1+
16. Nitrato de plata y wolframato sódico. Solubilización de los precipitados
(continuación).
Partimos del precipitado blanquecino amarillento de Ag2WO4,
figura 10, del tema 15.

Fig.10

Fig.16
Prácticamente ha desaparecido el precipitado
Pasan unas horas
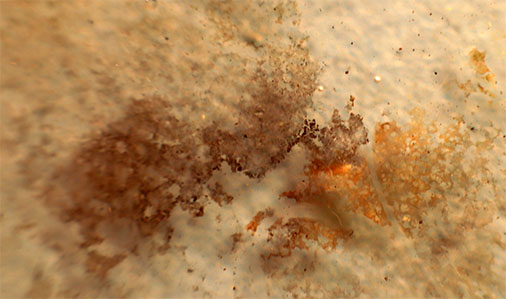
Fig.15

Fig.14

Fig.12

Fig.11
El proceso que tuvo lugar es:
2AgNO3 (ac)+ Na2WO4 (ac)= Ag2WO4(s)+
2NaNO3
Precipitado blanco amarillento
Vamos a agregarle
unas gotas de hidróxido amónico
La reacción que
tiene lugar es
El proceso que tiene lugar es:
Ag2WO4(s)+ 2NH4OH(ac)=
[Ag(NH3)2]2WO4(ac)+2H2O
Precipitado blanco amarillento
Con lo cual el precipitado
solubilizados tiende a desaparecer

Fig.13