
Fig.15
ENSEÑANZA DE LA FÍSICA Y LA QUÍMICA
PRECIPITACIÓN DE SALES DE Ag1+
14. Nitrato de plata y oxalato sódico. Solubilización de los precipitados (continuación)
Partimos del precipitado blanquecino amarillento de Ag2C2O4,
figura 11, del tema 13.

Fig.15
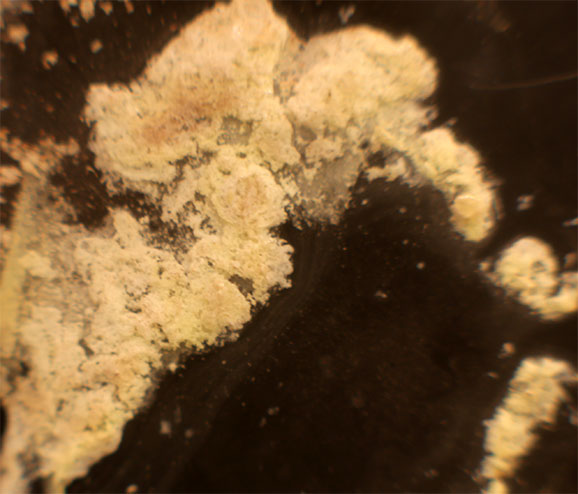
Fig.14

Fig.12
Vamos a agregarle
unas gotas de hidróxido amónico
El proceso que tiene lugar es:
Ag2C2O4(s)+
2NH4OH(ac)= [Ag(NH3)2]2C2O4(ac)+2H2O
Precipitado blanco amarillento
Con lo cual el precipitado
solubilizados tiende a desaparecer
Fig.16
El proceso que tiene lugar es:
2AgNO3 (ac)+ Na2C2O4 (ac)= Ag2C2O4(s)+
2NaNO3
Precipitado blanco amarillento
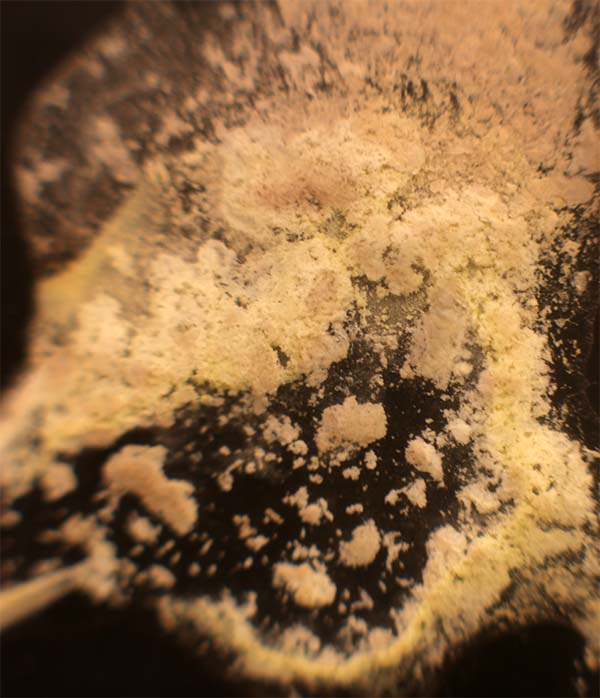
Fig.13

Fig.11