| INSTRUCCIONES GENERALES Y VALORACIÓN La prueba consta de dos
opciones, A y B, ambas con tres cuestiones y dos problemas. el alumno
deberá optar por una de las opciones, sin que pueda elegir problemas
y cuestiones de cada opción. Cada cuestión o problema puntuará sobre
un máximo de dos puntos. No se contestará ninguna pregunta en este
impreso. TIEMPO: una hora y treinta minutos |
| OPCIÓN A |
| Cuestión
1.- Prediga el efecto que puede causar en la solubilización
del cloruro de plomo (II )
a) Añadirle una disolución de nitrato de plomo. b) Incrementar su temperatura. c) Añadirle ácido clorhídrico. Puntuación máxima por
apartado: 0,75 a-0,75 b- 0,5 c |
| Cuestión
2.- Razone
si son ciertas o falsas las afirmaciones referidas a una disolución
acuosa de hidróxido amónico: a) Su grado de disociación es independiente de la concentración inicial de base b) Si se le añade una pequeña cantidad de hidróxido
sódico su grado de disociación aumenta. Puntuación máxima por
apartado: 1P |
| Cuestión
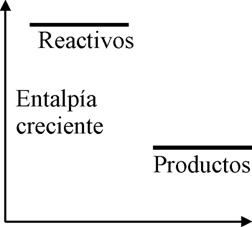
3.- El amoniaco es un gas, que se forma por síntesis
a partir de sus componentes, siendo dicha reacción exotérmica (-46kJ/mol) a) Razone las condiciones por las cuales se
podrá obtener mayor cantidad de amoniaco b) Es posible que pese a ser un gas presente
carácter básico. Justifique Puntuación máxima por apartado: 1P |
| Problema 1.-
a)
Una disolución acuosa de ácido nítrico
reacciona con sulfuro de hidrógeno(g) para dar azufre(s) y óxido nítrico(g).
Explique, ajuste la reacción y nombre todas las especies que intervienen
en la reacción
b)
Determine el volumen de sulfuro de
hidrógeno a 1 atm de presión
y 60ºC que se obtiene cuando
reaccionan 500cm3 de una disolución acuosa
de ácido nítrico 3N. DATOS: N=14, H=1, O=16, S=32,
R=0,082 atmL/K.mol Puntuación máxima por
apartado: 1P |
| Problema 2.- En la etiqueta de una botella de un litro de ácido clorhídrico figuran los siguientes datos: densidad=1,1g/cm3; riqueza 30 % Calcule: a) La Normalidad de dicha disolución. b) El volumen de hidróxido cálcico 2,0M necesario para que neutralice todo el ácido. c) El pH final si se aumentara dicho volumen en un 10% Puntuación
máxima por apartado: a) 0,75P- b) 0,75P- c)0,5P |