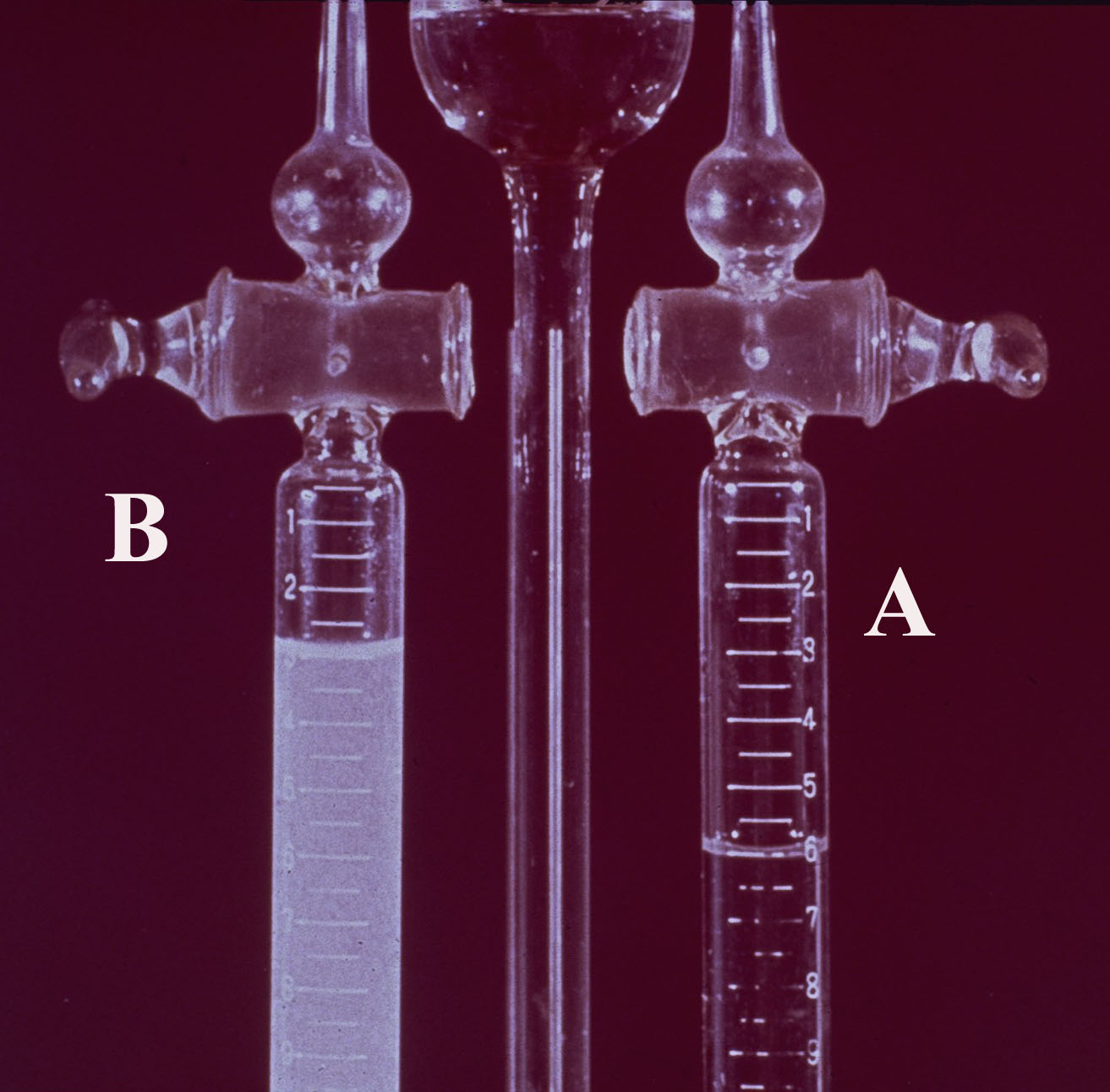
FOTO 1
ENSEÑANZA DE LA FÍSICA Y LA QUÍMICA
PROBLEMAS VISUALES DE QUÍMICA 7
PVQ7-1**
En A, se disponen 10 mL de H2SO4 2N y en B,
R= 0,082 atm-L.K-1 mol-1
a)
¿Qué
gas se recoge en el matraz? Formula la reacción
b)
Sobra
algún producto ¿Cuánto?
c) Qué volumen ocuparía el gas a 17ºCy 770 mmHg de presión
d) Si se dispone en D, (quitando la conexión que lleva al matraz C), un papel de tornasol humedecido ¿qué color tomaría? Justifícalo
Datos.Masas atómicas : Na=23, H=1, S=32, O=16
PVQ7-2**
El dispositivo de la fotografía 1, corresponde a los receptores de gas de un
voltámetro de Hofmann donde se realiza la electrólisis
de agua acidulada a
a) Qué se obtiene en A y B
b) Los electrones que han circulado por el dispositivo
c) Si el cronómetro de la foto 2 se pone a 0 al iniciar la electrólisis, cuál será la intensidad de la corriente continua
DATOS:
Número de Avogadro, NA= 6,022.1023 electrones/mol
R=0,082 atm-L.K-1 mol-1, H=1; O=16
Presión de vapor de agua a 20ºC=19,83mmHg
1Faraday=96487C=1 mol de electrones
En el cronómetro de la fotografía 2, la aguja blanca determina los minutos y la amarilla los segundos.
PVQ7-3**
En un vaso de precipitados dispones de:
A=50mL de disolución de CuSO4 0,5M, y B=una plancha de cinc, que pesó 7,52g (foto 1).
Al cabo de algún tiempo, la disolución A’cambia de color (foto 2) y la parte sumergida cambia de aspecto. La plancha BB’, pesó 7,50g (se pierde algo de producto en el fondo del vaso de precipitados). Separada definitivamente la plancha metálica de la disolución, y limpiada de agregados metálicos, toma el aspecto B’’(foto 3), pesando 7,32g. Se pregunta:
a) Las reacciones que han tenido lugar, indicando los producto de reacción
b) Las concentraciones finales de las disoluciones que aparecerán en el vaso de precipitados
c) Los gramos de cobre que aparecen en el fondo del vaso de precipitados en la fotografía 2
DATOS: Masas atómicas Cu=63,55; Zn=65,38; S=32, O=16.
Potenciales normales de reducción: Zn2+/Zn=-0,76V; Cu2+/Cu=0,34V

FOTO 1

FOTO1

FOTO 2


FOTO 2

FOTO 3