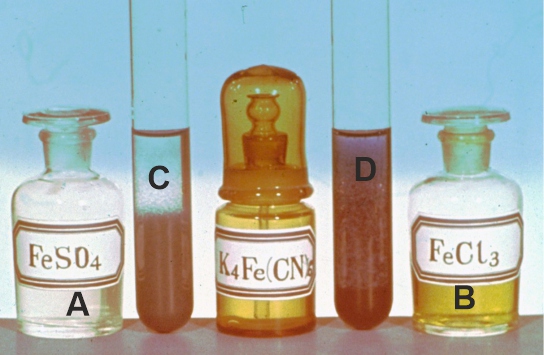
Fotografía 1
ENSEÑANZA DE LA FÍSICA Y LA QUÍMICA
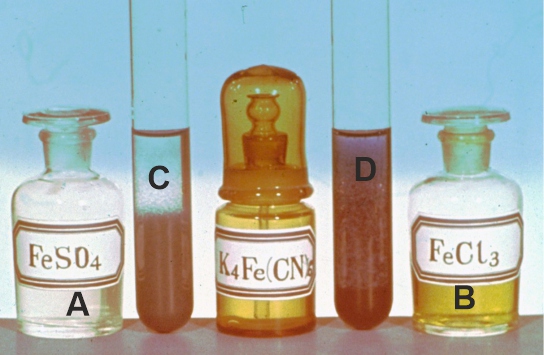
Fotografía 1

Fotografía 2
Dispones en A (foto 1) de una 20mL
de disolución de sulfato de hierro(II) 2M, a la que agregas en C, la misma
cantidad de ferrocianuro potásico. En D se realiza la misma operación con la
misma cantidad de cloruro de hierro(III) 2M, agregándose en todos los casos
agua destilada hasta completar 50mL y dando lugar a las fotos que se presentan.
En la fotografía 2, se realiza la misma operación con ferricianuro
potásico con los reactivos en A y B agregándose
en todos los casos agua destilada hasta completar 50mL y surgiendo las
reacciones respectivas en C y D
a) Formula las reacciones que tienen lugar en cada tubo de las dos fotos
b) En cuál de los recipientes C y D, de cada foto, habrá mayor concentración
de in ferroso.
c) En cuál de los cuatro tubos de ensayo habrá mayor concentración de ion
férrico.