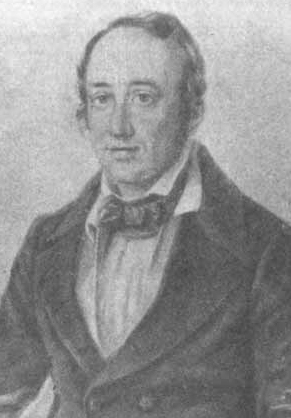
Germain Hess en San Petersburgo
ENSEÑANZA DE LA FÍSICA Y LA QUÍMICA
Germain Hess, el médico conocido por su ley termoquímica,
pero del cual se sabe poco mas.
Todos los estudiantes de enseñanzas medias, hay oído hablar de la ley de Hess, sin embargo pocos saben quien fue Germain Hess, y qué otras contribuciones hizo a la ciencia.
Aunque nace en Ginebra el 26 de junio de 1802, su padre se traslada a Rusia, para enseñar allí tres años después, por eso su formación y toda su vida transcurre prácticamente en ese país, y por eso es menos conocida, ya que todas biografías están escritas en ruso
A los 20 años, ingresa en la facultad de medicina de la universidad de Dorpat (actualmente la Estonia Tartu), una de las universidades mas prestigiosas de Rusia en aquel tiempo. Junto con la medicina también estudio química y geología, por eso para el grado de doctor en medicina presentó en 1825, una tesis sobre Estudio sobre la composición química y la acción medicinal de las aguas de Rusia.
Para mejorar su formación química, se va en 1826, a Estocolmo, a estudiar con Berzelius, el análisis químico, a fin de aplicarlo al descubrimiento de nuevos minerales en Rusia. De vuelta a su país de adopción y después de una expedición geológica a los montes Urales, se dedica a la medicina en Irkutsk, en plena Siberia, sin dejar de estudiar los minerales y aguas de esa región, estudio que llamó la atención de los académicos de San Petersburgo, que lo eligen en 1928, miembro de la Academia, y dos años después Académico extraordinario, ya en San Petersburgo, dedicándose plenamente a la química, comenzando como no, con el estudio de las aguas del río Neva, cerca de San Petersburgo.
Su actividad inicial es mucha. Descubre un mineral de cobalto, de composición Co3O4 (confirmado posteriormente por Berzelius). Analiza por primera vez el gas natural de Bakú, que sería después la principal fuente de petróleo de Rusia, y estudia la oxidación de los azúcares con ácido nítrico, obteniendo el ácido sacárico. Todos estos trabajos le llevan a que le encomienden el desarrollo de un curso de química teórica y práctica, en el nuevo Instituto Tecnológico de San Petersburgo, del cual será ya en 1832, su director pedagógico. Publica entonces su Fundamentos de Química pura en dos volúmenes. Este libro tiene la importancia de introducir la nomenclatura química que existía en Europa (procedente de la de Lavoisier), en lenguaje ruso. Dos años después publica otro texto más manejable, del cual se hicieron 7 ediciones. También en 1834, es hecho, por fin, Académico ordinario de la Academia de Ciencias de San Petersburgo.
En 1838, comienzan sus investigaciones sobre el calor desarrollado en las reacciones químicas. Calcula el calor de hidratación del ácido sulfúrico, a partir de la formación de sus diferentes hidratos y lo publica con el título:La evolución del calor en proporciones múltiples. Dos años después aparece escrita en francés, en el Boletín de la Academia de Ciencias de San Petersburgo, y en alemán en los Annalen de Física y Química, su primera ley, la conocida como ley de Hess, con el nombre de Ley de la suma constante del calor. Señalando que no solo en los hidratos del ácido sulfúrico, sino también en las neutralizaciones con hidróxido amónico para formar sulfato de amonio, y en las neutralizaciones del ácido clorhídrico con hidróxidos sódico y potásico, la cantidad de calor desarrollada es siempre la misma, ya se calcule directamente, ya se haga en varios pasos [1] . Hess era consciente de la importancia de su ley, así como de sus posibles aplicaciones, sin embargo pese a publicarla en francés y en alemán, no tuvieron repercusión hasta que Ostwald, en 1887, en su Textbook of General Chemistry, publicó un capítulo dedicado a la termoquímica, en el que revindicó la importancia y contribuciones de Germain Hess.
Germain Hess en San Petersburgo
También determina Hess el poder calorífico del carbón, en función de la cantidad necesaria de oxígeno para que pudiera arder.
En 1842, publica su segunda ley; la Ley de la electroneutralidad, en la cual indica que en las reacciones de intercambio iones en las sales neutras, no se observan efectos caloríficos. La explicación de esta ley se hará mas tarde a partir de la disociación electrolítica de Arrhenius.
En 1848,
su salud decae, y se retira de la enseñanza. Su última actividad pública,
fue una visita de inspección a las nuevas factorías de refinamiento de azúcar
inauguradas en el sur de Rusia. Fallece el 30 de noviembre de 1850, a los
48 años.
[1] Es importante señalar que esta afirmación basada en hechos experimentales, se adelantó en dos años al principio de Conservación de la energía enunciado por Meyer en 1842.