ENSEÑANZA DE LA FÍSICA Y LA QUÍMICA
LOS METALES DE LA TIERRA: LITIO
Y CADMIO
Estamos en 1817, y por esas fechas
se conocía un mineral muy curioso, llamado espodumeno, cuyas disoluciones
comunicaban a la llama un intenso color rojizo, sin saberse el motivo. Vauquelin
analiza a principios de siglo el mineral para intentar explicar aquellos
hechos y supuso la existencia de algún elemento desconocido, pero no logró
aislarlo. En su composición había un 9,5% de sustancia desconocida; suponía
se trataba de un álcali. Al año siguiente, un alumno de Berzelius, Juan
Augusto Arfwedson analiza la petalita, un mineral sueco descubierto por
el brasileño Andrade e Silva508,
que da este resultado:
Sílice 80% Alúmina 17%
Sustancia metálica desconocida 3%509.
Esta sustancia metálica era una
cal u óxido de un nuevo metal. Así lo describe Berzelius, en 1818, en carta
de 9 de febrero a su colega francés
Berthollet:
"El nuevo álcali, lo descubrió
el Sr.Arfwedson, un joven químico muy avispado que ha estado trabajando
un año en mi laboratorio. Encontró este álcali en una roca descubierta previamente
por el Sr. d'Andrada en una mina de Utö, y denominada por él petalita. Esta
roca contiene en números redondos 80% de sílice, 17% de alúmina y 3% del
nuevo álcali. Tiene una mayor capacidad para neutralizar ácidos que los
demás álcalis fijos e incluso sobrepasa a la magnesia. Se descubrió precisamente
por esta circunstancia pues la sal que da el álcali como base, que se obtuvo
en la marcha del análisis excede en mucho al peso que debería tener, si
la base hubiera sido sosa o potasa. Era muy natural imaginar que una sal,
con una base alcalina, que no precipita nada con ácido tartárico, contuviera sosa. Así lo supuso
Arfwedson al principio, pero al repetir el análisis de la petalita por tres
veces exactamente con los mismos resultados, pensó que debía examinar cada
constituyente con más detalle y fue a consecuencia de tal examen que observó
que la sustancia alcalina poseía propiedades diferentes de las demás álcalis.
Hemos dado a este álcali el nombre de LITHIA o LITINA, para
recordar que se descubrió en el reino mineral mientras que los otros se
descubrieron en el vegetal"510.
La carta anterior, se anticipó
en casi un año, a la Memoria publicada por el propio Arfwedson, en la que
se anunciaba el descubrimiento de la tierra que debería contener un nuevo
elemento químico511. Sin embargo,
aunque descubrió su óxido, Arfwedson no fue capaz de aislar el metal, ni
aun empleando medios electroquímicos, pues la pila de que disponía no tenía la potencia adecuada.
Ese
mismo año, Davy consiguió aislar el metal, sometiendo a electrólisis ígnea
a su carbonato512; igualmente
lo hace Brande, poco después. Realmente el nombre del metal aparece en la
descripción de los experimentos de Brande, como se puede ver:
"Al someter la LITHIA a la
acción de la pila voltaica se descompone con el mismo fenómeno que la potasa
y la sosa. Se separa una sustancia metálica, blanca, brillante, altamente
combustible que al aplicar el término de LITHIA al óxido puede ser llamada
LITHIUM. Las propiedades de este metal no se han investigado hasta
ahora a consecuencia de la dificultad de procurarse su óxido en alguna cantidad".
Por lo tanto, el nombre del elemento
LITHIUM, procederá del griego LITHOS (λίθoς,
piedra), término de etimología dudosa (no aparecen analogías en otras lenguas
indoeuropeas), conservándolo en las demás lenguas, a diferencia de sus hermanos,
los otros elementos alcalinos. Sus propiedades no fueron muy estudiadas,
pues hasta 1855, no se consiguió suficiente cantidad del metal puro.
Su nombre proviene de haberse encontrado
únicamente en el reino mineral, esto es, en las piedras, minerales tales
como la petalina y el espodumeno. Mal había de saberse el papel importantísimo
que desempeña en el reino animal, en el que su ión debido al pequeño tamaño,
puede penetrar fácilmente por los canales iónicos celulares, desempeñando
un aspecto regulador en el sistema nervioso, de tal forma que su carencia
implica la generación de estados depresivos, tan habituales en la vida moderna.
El último metal del grupo, el CADMIUM
o CADMIO en español, va a presentar nada menos que cinco descubridores
simultáneos, que ofrecen nuevos nombres para el elemento. Así aparte de
CADMIUM, va a ser VESTIUM según Gilbert, en 1818;
VESTALIUM, según von
West en 1818; JUNONIUM, según Thomson en 1811; MELINIUM y KLAPROTHIUM. Como podemos
observar la latinización no fue seguida por todos los científicos. Los tres
primeros de origen astronómico. En
recuerdo de los asteroides VESTA
y JUNO, descubiertos por Hardings y Olbers entre 1804 y 1807,
siguiendo la moda iniciada por el PALLADIUM y el CERIUM513. El MELINIUM,
del griego MELOS (μηλoς, negro), se debe a la
coloración de sus sales fundidas. El último es honorífico, en recuerdo del
científico alemán que había fallecido en enero de ese mismo año.
Sólo perdurará el CADMIUM
propuesto por Federico Stronmeyer, profesor de Gottinga, por haberlo encontrado
por casualidad en el mineral CADMIA, del que ya hemos hablado en
la etimología del cinc514.
Era inspector farmacéutico, y visitando en 1817, una en Hildenheim, encuentra
un carbonato de cinc (CADMIA o CALAMINA), que se vuelve naranja
al calentarlo, hecho que le llamó poderosamente la atención515. )Cómo consiguió aislar el metal? Nada de métodos electroquímicos, no hacían falta; llegaba
con una marcha analítica rutinaria. Disolvió el óxido de cinc procedente
de la cadmia, en ácido sulfúrico, y después lo precipitó como sulfuro al
pasar corriente de sulfuro de hidrógeno. Lavó el precipitado y lo disolvió
en ácido clorhídrico concentrado, evaporando a sequedad para eliminar el
exceso de ácido. Vuelve a lavar con carbonato amónico para extraer el cinc
y el cobre. El carbonato del elemento desconocido no era soluble. Una vez
que lo filtró y calcinó, redujo el óxido parduzco con carbón en una retorta,
calentando hasta el rojo poco a poco. Al terminar encontró en el fondo del
recipiente un botón metálico brillante, de un color gris azulado.
Stronmeyer no fue el único que
aisló el cadmio. Su inspección farmacéutica en otros estados alemanes había
separado partidas de preparados de cinc, que procedían de la fábrica de
Schönebeck, por sospechar llevaban impurezas de arsénico, pues el precipitado
con sulfuro de hidrógeno era amarillo, tal como el oropimente. La investigación
de los químicos de la propia fábrica516,
no encontraron arsénico, pero sí
una sustancia nueva, que coincidía con la aislada de la cadmia.
El MELINIUM no se justifica
realmente pues todas las combinaciones del CADMIO son blancas o de colores claros, como se corresponde
a un elemento que en estado de oxidación (2+), tiene su último
nivel completo (4s2 4p6 4d10), con lo que
la absorción energética sería en el ultravioleta, apareciendo como reflejado
el blanco. La única explicación posible es que se hubiera obtenido con impurezas,
o a través de sulfuros.
La otra confusión fue su posible asociación con el sulfuro de arsénico (oropimente), por culpa de su color amarillo. Por eso vamos a justificar por qué a diferencia de otros muchos sulfuros de metales divalentes (pardo oscuros), el sulfuro de cadmio tiene color amarillo, color que fue el punto de partida para su descubrimiento.
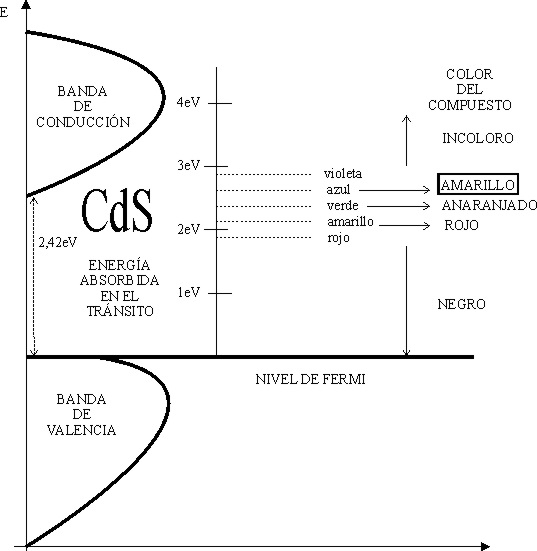
En capítulos anteriores se ha explicado la teoría del color en sólidos, a través de las transiciones electrónicas entre las diferentes bandas.
El sulfuro de cadmio, que precisamente se emplea como pigmento pictórico con el nombre de "amarillo de cadmio", tiene un intervalo de energías prohibidas, entre la banda de valencia y la de conducción, de 2,4 electrón voltios (517nm), lo que le hace absorber solamente en el azul y violeta. Al eliminar estas longitudes de onda de la luz blanca, la radiación que emite corresponde al amarillo. Simplemente sustituyendo el S por otro elemento similar pero más voluminoso, como el selenio, ya varía la separación entre las bandas.
Así en el seleniuro de cadmio, la separación es de sólo 1,8 eV, con lo cual absorbe todo el espectro visible menos aquella parte de menor energía (correspondiente al rojo), por ese motivo este compuesto es rojo

508 Era un mineral difícil de fundir,
con aspecto laminar, en forma de pétalos de flores (de ahí su nombre),
que se disolvía sin efervescencia en ácido nítrico. También describió y bautizó el espodumeno, basándose
en un antiguo mineral, el spondium, que aparecía en las menas del cinc.
509 Antes que Arfwedson, Vauquelin
había efectuado un análisis semejante, pero supuso que la sustancia alcalina
desconocida, era potasa. antes. En el mismo año, el inglés Clarke obtuvo
en dicho análisis una "pérdida de masa" del 1,75%.
510 Hacía referencia al descubrimiento
del sodio y del potasio realizado por Davy con los procedimientos electrolíticos.
511 En 1821, publicó un suplemento
a su Memoria, en la que afirmaba que la sal que se había formado entre el sulfúrico y la
lithia, y que había supuesto se
trataba de una sal ácida, se trataba de una sal normal, y que el sulfato
doble que había tomado como un alumbre del nuevo elemento, era realmente
alumbre potásico.
512 Lo relata así: "Se descompuso
el álcali con brillantes chispas y al separar el metal reducido, se inflamó.
Las pequeñas partículas eran semejantes a las de sodium. Un glóbulo de
mercurio al que se le dio carga negativa, y se puso en contacto con la
sal alcalina, se convirtió en amalgama y pudo reaccionar con el agua...".
513 Entre 1801 y 1807, se descubrieron
los 4 primeros asteroides del sistema solar, por aplicación de la ley
de Titius-Bode, lo cual causó gran conmoción en el mundo científico. Piazzi,
primero y Olbers después, comienzan con Ceres. Poco después será Pallas.
En 1804, Harding y Lilienthal, Juno, y por fin en 1807, Olbers, identifica
a Vesta. El quinto no surgirá hasta 1845, con el nombre de Astraea. Es
curioso que sus nombres apenas se recuerden, y sin embargo "bautizaron"
a 3 o 4 nuevos elementos del sistema periódico, CERIO, PALADIO, VESTIO
O VESTALIO, Y JUNONIO, aunque estos últimos no prevalecieran; fue la moda
astronómica.
514 Debe recordarse que Cadmo, en
la mitología griega, fundador de Tebas, era el "hombre venido de
oriente", en este caso, de las costas fenicias, por eso a los caracteres
arameos, se les denominan fenicios
o cadmeicos.
515 Lo cuenta así en una carta fechada
el 26/04/1818, dirigida al Prof. Schwigger: "Mientras en el otoño
último inspeccionaba las boticas del principado de Hildesheim, por haberme
confiado nuestra muy graciosa Regencia, la inspección general de las farmacias
del reino, observé en algunas, en vez del adecuado óxido de cinc, un carbonato
de cinc que procedía casi totalmente de la fábrica química de Saltzgitter.
Este carbonato tiene un color blanco deslumbrante, pero cuando se calienta
al rojo toma un color amarillo ligeramente anaranjado, a pesar de que
no se puede hallar en él ninguna cantidad apreciable de hierro o plomo.
Cuando visité la factoría química y expresé mi sorpresa de que se hubiera
vendido carbonato de cinc, en vez de óxido de cinc, el
encargado, Sr.Jost me informó que la razón era que su carbonato
de cinc al someterlo al calor del rojo adquiría siempre el tono amarillo
y que se suponía que contenía hierro, aun cuando se había tenido el mayor
cuidado de librar de antemano el cinc del hierro y a pesar de no haber
podido encontrar hierro en el propio óxido de cinc. Esta información me
indujo a examinar el óxido de cinc con mayor cuidado y encontré con gran
sorpresa mía que el color que adquiría se debía a la presencia de un óxido
metálico peculiar, cuya existencia no se había sospechado hasta ahora".
516 Los otros descubridores del
cadmium, serán el químico Dr. Hermann
y el médico Roloff.