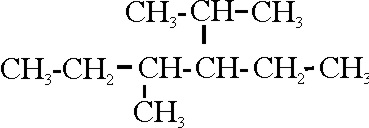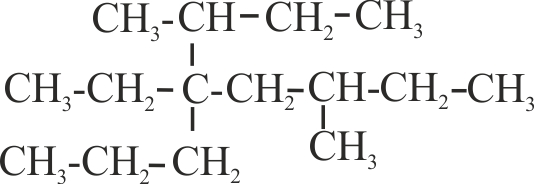
ENSEÑANZA DE LA FÍSICA Y LA QUÍMICA

FORMULACIÓN ORGÁNICA 1
10.1. Pese a que a Berzelius siempre se
le atribuyó la paternidad del nombre de química orgánica, realmente, 30 años
antes, otro químico sueco, Bergmann, ya había realizado la división de la
química, en inorgánica y orgánica, o química del carbono. El carbono, nuestro
protagonista, se puede encontrar en las diferentes cadenas, unido a 1,2,3 y 4
carbonos, y así podrá ser primario, secundario, terciario y cuaternario,
variando su reactividad y la energía de sus enlaces. Así, en el esqueleto de
carbonos adjunto, que deberás numerar y estructurar, podrás decir que:
a)
Hay 8 carbonos primarios
b)
Solo existe 1 carbono secundario
c)
Hay 4 carbonos terciarios
d)
Solo existe 1 carbono cuaternario
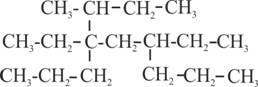
10.2. A
finales de julio de abril de 1889, se celebra en Paris, una conferencia previa
a la de Ginebra sobre nomenclatura orgánica. En ella se adscribió a todos los
alcoholes el sufijo ol y se determinó, por sugerencia del profesor Behal,
considerar la cadena principal que determinaría el prefijo del nombre del
compuesto a la sucesión de carbonos mas larga de esta forma dado el
hidrocarburo saturado de la figura
podrías asegurar que se trata de un:
a) Heptano b) Octano c)
Nonano d) Decano
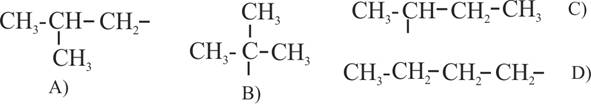
10.4. Cuando lees fórmulas orgánicas, te encuentras
que las ramificaciones se escriben delante de la cadena principal, y algunas
de ellas no siguen una nomenclatura sistemática, sino que se efectúa por el
número de carbonos, especificando ya el tipo de carbono que realiza la
inserción, o la estructura ramificada de aquella. Por eso de los radicales
dados y numerados podrás decir que:
a) el C es un n-butil
b)
el D es un sec-butil, o también 2-metilpropil
c) el B es un terc-butil, o también 1,1-dimetiletil
d) el A es un iso-butil, o también 1-metilpropil
10.5. El radical
dado en el cuadro se llamó antiguamente acetilenil. Sólo a partir de 1950 se le
denominó:
a) acetenil b)
etinil c)
acetinil d)
etil
![]()
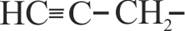
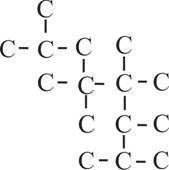
10.6. El radical
dado en el cuadro se llamó antiguamente propargil, formado por el prefjo prop,
que recuerda su origen del propino y el sufijo argil, procedente del argentum latino, ya que el ion plata, intervenía como catalizador en la sustitución del hidrógeno ácido, para
posteriores síntesis. Sólo a partir de 1950 se le denominó:
a)1-propinil b)2-propinil c) propionil d) propinilideno
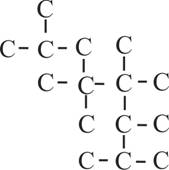
10.7. Según las reglas actuales de la
IUPAC, el hidrocarburo saturado cuyo esqueleto carbonoso te dan, debería
llamarse:
a) 2,4,5,5,6,6,7-heptametiloctano
b)2,3,4,4,5,5,7-heptametil-octano
c)1,1,2,3,4,4,5,5-octametilheptano
d)2,4,5,5,6,6,7,7-octametilheptano
10.8.El hidrocarburo cuyo esqueleto
carbonado te dar debería llamarse según la nomenclatura actual:
a)
2,2-dimetilbutano
b)
3,3,3-trimetilpropano
c)
isohexano
d) terc-hexano
10.19. La
nomenclatura de Ginebra, tenía reglas muy curiosas, puesto que en la numeración
de la cadena principal, predominaban los radicales hidrocarbonados sobre
cualquier otro, con lo cual el compuesto dado se denominaba
metil-2-cloropentano 4, al numerarse desde la izquierda.
Actualmente se denominaría:
a)2-metil-4-cloropentano b)
4-metil-2-cloropentano
c) 2-cloro-4-metilpentano d) 4-cloro-2-metilpentano
10.9.El
hidrocarburo cuyo esqueleto carbonado te dar debería llamarse según la
nomenclatura actual:
a)2-etinil-2-metilbutano
b)3,3-dimetil-1-pentino
c)3-etil-3-metil-1-pentino
d)1-heptino
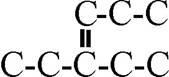
10.11. Los
estudiantes suelen usar modelos moleculares para comprender mejor la estructura
espacial de las moléculas orgánicas. Lo que pocos saben es que fue Hofmann el
primero en hacerlo empleando pelotas de croquet, en 1865. Igualmente, este
mismo científico fue el que propuso al año siguiente los sufijos ene, ino y
ono derivador del griego con el
significado de hijos de, para los hidrocarburos con enlaces sencillos, dobles y
triples, que después cambiaría por ane, ene e ine (ano, eno e ino en español).
En estos hidrocarburos, las reglas de la IUPAC,
seguidas actualmente, inciden en que la cadena principal de un hidrocarburo
alcano, debe ser la más larga, y comenzará a numerarse de forma que al radical
más pequeño le corresponda la numeración inferior. Por eso el esqueleto
carbonoso del hidrocarburo saturado que te dan, deberá corresponder al:
a) 2,
3, 4, 5-tetrametilheptano b)
5-etil-2, 3, 4-trimetilhexano
c) 3,
4, 5, 6-tetrametilheptano d)
3, 4-dimetil-5-metiletilhexano
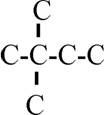
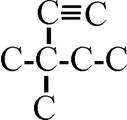
10.10*.El hidrocarburo cuyo esqueleto
carbonado te dan se debería llamar-se según la nomenclatura actual:
a)4-etil-3-hexeno b)3-propilidenopentano
c)3-etil-3-hex-3-eno d)3-etil-3-hexeno
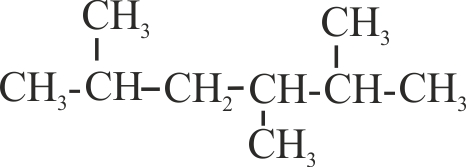
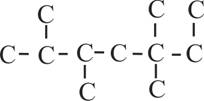
10.12*.Las primeras reglas
internacionales de nomenclatura orgánica fueron elaboradas en Ginebra, en 1892,
sin embargo y para intentar homogeneizar los criterios de químicos de
diferentes países, sufrió numerosas modificaciones, desde la reunión de la
IUPAC (Unión Inter-nacional de Química Pura y Aplicada), organismo creado
precisamente para ello, en Lieja en
1930, hasta nuestros días. Actualmente el nombre de un compuesto orgánico
sencillo consta de un núcleo formado por un prefijo indicativo del número de
carbonos que lo integran y un sufijo que especifica la o las familias a que
corresponden, precedido de un número localizador que nos indicará la
posición de la función representativa.
Así si un compuesto está formado por 5 carbonos, y dos
dobles enlaces sucesivos en el medio de la cadena y, teniendo en cuenta la tabla
adjunta deberíamos denominarlo:
a) dipenteno-2,3 b) pent-2,3-dieno
c)
3,4-pentadieno d) 2,3-pentadieno
|
|
![]()
10.15*.Las
conclusiones de la conferencia de
Ginebra de 1892, sobre nomenclatura orgánica, se redactaron en francés, ya que
su presidente el profesor Friedel, era catedrático en La Sorbonne. Por ese
motivo, la regla sobre posición de los localizadores de funciones y radicales,
que era indefinida, se aplicó con los localizadores detrás de la función.
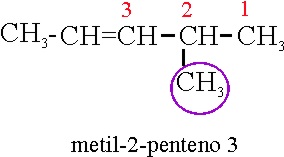
Al mismo tiempo,
mandaba a la hora de numerar la cadena principal, la función hidrocarburo, por
eso el compuesto cuya estructura te dan
se denominó metil-2-penteno 3. Sin embargo actualmente se debería llamar:
a) metil-4-penteno-2 b) 4-metil-pent-2-eno
c) 4-metil-2-penteno d) 2-metil-3-penteno
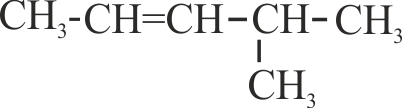
10.13*. Aunque
Hofmann no asistió a la conferencia sobra nomenclatura orgánica de París, en
1889, si se presentó también la
propuesta de denominar con el sufijo uno aquellos hidrocarburos con dobles y
triples enlaces acumulados.
De esa forma la fórmula presentada se debería llamar
butuno. Con las normas actuales su nombre sería:
a) but-1-eno-3-ino b)1-buteno-3-ino
c) 3-butino-1-eno d)
1-butino-3-eno
10.14*. No todos
los radicales orgánicos terminaban en il o ilo. Los que estaban unidos por un
doble enlace, antes de 1949, se denominaban, si tenían 1, 2 carbonos etc:
meten, eten etc. Fue en la conferencia de Amsterdam, de 1949, cuando se acordó
caracterizarlos por el sufijo ilideno, o ilidino si hubiera un triple enlace. Por
este motivo y teniendo en cuenta las reglas de formulación y preferencias, del
hidrocarburo cuya fórmula te dan dirás que:
a) Existe un metilideno en el carbono 3
b) En el carbono 2 hay un metil
c) Del carbono 3,sale una ramificación
etenil
d) La cadena principal tiene 4 carbonos
|
|
10.16.Aunque
muchos se creen que la conferencia de Ginebra fue determinante en la nomenclatura
orgánica, sin embargo, el nombre del
compuesto dado según dicha nomenclatura , en el segundo cuadro de la izquierda,
no se parece con el que darías las reglas actuales, pues según ellas se
llamaría:
a) 2,4-dimetil-3-etilhexano b) 3-etil-2,4-dimetilhexano
c) 3-metil-4-isopropilhexano d)3-isopropil-4-metilhexano
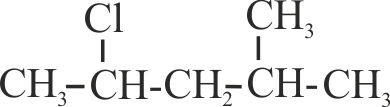
10.17. Aplicando
las normas aprobadas en la conferencia de Ginebra de 1892, el compuesto dado a
la izquierda, se nombraría como se indica, esto es comenzando a numerar la
cadena de forma que al metilo le correspon-diera el número mas bajo sin embargo
actualmente se denominaría:
a) 2-metil-penteno-3 b) 2-metil-3-penteno
c)4-metil-2-penteno d)4-metilpent-2-eno
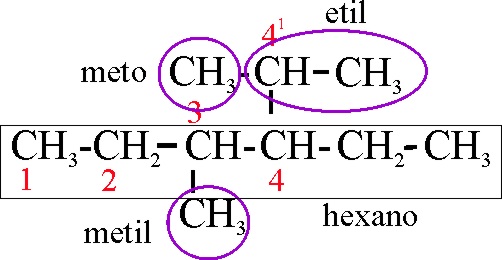
10.18. Las regla
A-2-1 y A-2-2, de la IUPAC, determinan
como han de nombrarse los hidrocarburos con ramificaciones. En el caso del
compues-to dado, se juntan las ramificaciones con un prefijo multiplicativo
pero al numerar la cadena deberá hacerse de forma que la suma de localizadores
sea la mas baja posible por ello el nombre del compuesto será:
a) 2,4,5-trimetilhexano b)
2,3,5-trimetilhexano
c) 2,4,6-trimetilhexano d)2,3,6-trimetilhexano
10.20. En 1971, se aprobaron las normas que
permitieron introducir los paréntesis en los radicales complejos, pero claro,
la introducción de un nombre complejo, implica regular la alfabetización,
considerando únicamente la primera letra del nombre completo ( Regla A-2.3ii de
la IUPAC), por ese motivo el compuesto dado, debería llamarse:
a) 4-secbutil-4-etil-6-metiloctano
b) 5-etil-5-secbutil-3-metiloctano
c) 5-etil-3-metil-5-(1-metilpropil)octano
d) 5-metil-3-(1-metilpropil)-3-propilheptano